アルカプトン尿症
(Alkaptonuria)
[Synonyms: Alcaptonuria]
Gene Reviews著者: Wendy J Introne, MD, Michael A Kayser, DO, William A Gahl, MD, PhD
日本語訳者: 吉村祐実(ボランティア翻訳者),櫻井晃洋(札幌医科大学附属病院遺伝子診療科)
GeneReviews最終更新日:2021.6.10. 日本語訳最終更新日: 2022.8.25.
原文 Alkaptonuria
要約
疾患の特徴
アルカプトン尿症は、チロシン代謝経路でホモゲンチジン酸(HGA)をマレイルアセト酢酸へ変換する酵素であるホモゲンチジン酸-1,2-ジオキシゲナーゼの欠損により発症する。アルカプトン尿症の3大特徴は、暗褐色尿または放置後に暗褐色になる尿、組織色素沈着(結合組織の帯青黒色の色素沈着)、および脊椎と大関節の関節炎である。組織色素沈着は通常、30歳以降に発症する。関節炎はしばしば20歳代に始まる。その他の症状には、強膜、耳の軟骨、手の皮膚の色素沈着、大動脈弁または僧帽弁の石灰化または逆流、および場合によっては大動脈拡張、腎結石、前立腺結石、甲状腺機能低下症などがある。
診断・検査
発端者のアルカプトン尿症の生化学的診断は、尿中の多量のHGA(通常は1日あたり1〜8 g)の検出に基づく。
分子診断(家族に遺伝カウンセリングを提供するために必要)は、HGDにおける両アレルの病原性バリアントの同定によってなされる。
臨床的マネジメント
症状に対する治療:
患者に合わせた対症療法となる。関節痛の治療;筋力や柔軟性を維持するための理学療法および作業療法;適宜、膝、腰、肩の関節置換術;適宜、前立腺結石や腎結石に対する外科的処置。大動脈弁狭窄症は、弁置換術を必要とする場合がある。甲状腺ホルモンの補充。
症状の進行を遅らせることが示されているニチシノンがアルカプトン尿症の治療薬として欧州で承認されているが、米国では承認されていない。(訳注:日本では未承認)
経過観察:
40歳以上になると、大動脈拡張、大動脈弁や僧房弁の石灰化や閉鎖不全を検出するための心エコー検査;示唆的所見のある患者に対する冠動脈の石灰化を検出するCT検査。最初の診断時に甲状腺機能の評価、およびその後1~2年毎のモニタリング。
回避すべき薬剤や環境:
関節炎の重症化を避けるため、重労働や衝撃の大きいスポーツなどの脊椎や大関節への物理的ストレスを回避すること。
発症リスクのある血縁者への検査:
全体的な関節の可動性と機能を維持するのに役立つ予防措置の恩恵を受ける人をできるだけ早く特定するために、一見無症状の同胞を評価することは適切である。
遺伝カウンセリング
アルカプトン尿症は常染色体潜性遺伝(劣性遺伝)性疾患である。両親がHGD病原性バリアントについてヘテロ接合であることが同定されている場合、患者の同胞は、受胎時に25%の確率で罹患し、50%の確率で無症候性の保因者であり、25%の確率で無症状かつ保因者でもない。家族内で両方のHGD病原性バリアントが同定されている場合、リスクのある親族の保因者検査と出生前/着床前遺伝子検査が可能である。
診断
アルカプトン尿症に対する意見の一致した臨床的診断基準は公表されていない。
示唆的所見
以下の臨床的所見および家族歴を有する場合、アルカプトン尿症を疑うべきである。
臨床診断
- 暗色尿または放置した尿が暗色になる。尿中に排泄されるHGA酸化物がメラニン様産生物を作り出し、放置した際もしくはアルカリ性物質に触れると暗褐色となる。しかし、排尿後数時間は暗褐色化が起こらないため、多くの患者は尿に異常色を観察することがない。
- 組織色調変化(結合組織の帯青黒色の色素沈着).結合組織中のHGA蓄積およびHGA酸化物(ベンゾキノン酢酸など)による組織色調変化が起こる。
- 強膜の褐色色素沈着が角膜と外眼角と目頭の間の直筋付着部に認められる。色素沈着は結膜や角膜にも認められることがある(図 1A)。色素沈着は視力に影響しない[Chévez Barrios & Font 2004]。
- 耳介軟骨の色素沈着は、耳甲介や対耳輪に認められる(図 1B)。軟骨は灰色がかった青色(slate blue)もしくは灰色となり、不整形と感じる、または厚みを帯びたと感じられる。X線画像で耳介軟骨の石灰化がみられることもある。
- 耳垢や汗に色素が出て、衣服が変色することもある。
- 腱の色素沈着のために、手の皮膚や第1指と第2指の間が深紫や黒に変色することがある。
- 関節炎. 関節炎は脊椎から発症することが多く、病変が大関節に認められる点が強直性脊椎炎に類似する。脊髄のX線画像で認められる椎間板の平坦化や石灰化がこの疾患の特徴である(図1C)。臨床所見には、椎間板の石灰化後の椎間板変性から最終的な椎体の融合に至るまでが含まれる。骨棘の形成と椎間靭帯の石灰化も起こる。大関節のX線画像では関節空隙の狭隘化、肋軟骨下嚢胞、および骨棘の形成が認められる場合もある。筋肉付着点で腱付着部症が認められる場合がある[Mannoni et al 2004]。
注: 慢性的な関節痛で診察を受けた際、または整形外科手術中に黒い関節軟骨が認められた後にアルカプトン尿症の診断を下される患者もいる。
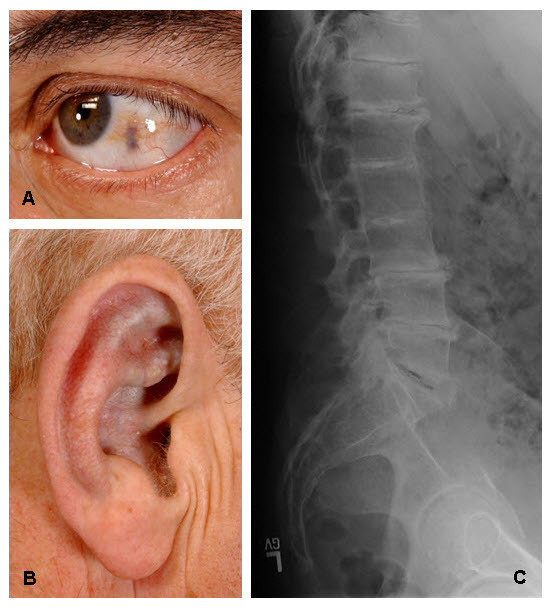
図 1
A. 眼の強膜における組織褐変
B. 耳甲介および対輪における組織褐変
C. 椎間板の平坦化、石灰化、および骨棘形成を伴う腰椎の典型的なX線所見
家族歴は常染色体潜性遺伝形式と一致する(例えば、罹患した同胞および/または親の血族結婚)。既知の家族歴がなくても、診断が妨げられることはない。
診断の確定
生化学検査
アルカプトン尿症の生化学検査による診断は、発端者に示唆的な臨床所見があること、ガスクロマトグラフィ-質量分析法で高い尿中HGA値が認められること、または液体クロマトグラフィータンデム質量分析に基づいて行われる。アルカプトン尿症患者のHGA値の1日排泄量は通常1~8gである。24時間尿でのHGA正常値は20~30mgである。(注:HGA値の上昇は、随時尿検体においても検出可能)
分子診断
アルカプトン尿症の分子診断は、分子遺伝学的検査によって同定されたHGDの疑いのある所見および両アレル病原性バリアントを有する発端者で確立される(表1を参照)。発端者のアルカプトン尿症の確定診断に分子遺伝学的検査は不要であるが、家族に遺伝カウンセリングを提供するために必要である(遺伝カウンセリングを参照)。
単一遺伝子検査
臨床検査でアルカプトン尿症と確定診断された場合、単一遺伝子検査が使用される。小規模な遺伝子内欠失/挿入やミスセンス変異、ナンセンス変異、スプライス部位変異を同定するためにHGDのシークエンス解析が最初に実施される。
表1. アルカプトン尿症の分子遺伝学的検査
| 遺伝子1 | 検査方法 | この方法で同定される病的バリアント2の割合 |
|---|---|---|
| HGD | シークエンス解析3 | 97%4 |
| 遺伝子標的欠失/重複解析5 | 3%4 |
- 表A 「遺伝子ならびに染色体座およびタンパク質のデータベース」を参照
- この遺伝子で同定されるアレルバリアントについては「分子遺伝学」を参照
- シークエンス解析では、benign, likely benign, of uncertain significance, likely pathogenic, or pathogenicのバリアントを同定する。バリアントには小さな遺伝子内欠失/挿入やミスセンス変異、ナンセンス変異、スプライスバリアントを含む。通常、エクソンまたは遺伝子全体の欠失/重複は検出できない。
- Vilboux et al [2009], Ascher et al [2019]
- 欠失/重複を標的とした遺伝子解析は遺伝子内欠失または重複が検出可能である。定量PCR法、ロングレンジPCR、MLPA法、単一エクソンの欠失・重複検出のために設計されたマイクロアレイなどが用いられる。
臨床的特徴
臨床所見
アルカプトン尿症の臨床所見には、結合組織の組織褐変、脊椎や大関節の関節炎がある。HGA排泄量と疾患の重症度は同一家系内でも大きなばらつきが認められることがある。アルカプトン尿症患者は発達障害や認知障害を起こすことはなく、通常、患者の寿命は減らない。
結合組織 一般に、色素的な変化が認められるのは30歳以降である。アキレス腱の肥厚化、腱炎、腱断裂などの腱関連症状も臨床的に認められ、MRI画像でもみることができる。
関節 組織黒変症を伴う関節炎はアルカプトン尿症で長期的に認められる一般的症状である。脊椎を含む関節症状は通常20歳代に生じる。ある大家系では腰痛が30歳以前の49%に、40歳以前では94%に認められた。
腰椎や胸椎症状は頸椎症状の前に現れる。一般に、仙腸骨部は侵されない。脊椎の柔軟性の低下が疾患の重症度と直接的な相関がある。前方への柔軟性が低下した患者は機能障害を呈し、疲労感が増す。
外科的介入を要したミエロパチーの症例報告のレビューにおいて、最も多かったもの部位から順に、頸椎、胸椎、および腰椎であった[Donaldson et al 2019]。
腰椎と胸椎の症状は頸椎の症状より早期に発現する。一般に、仙腸骨部は侵されない。脊椎の柔軟性の低下が疾患の重症度と直接的な相関がある。前方への柔軟性が低下した患者は機能障害を呈し、疲労感が増す仙骨領域は通常、症状が出ない。
関節症状は疾患初期に生じ、女性と比べ男性で進行速度が速いようである。膝、腰、肩の症状が多い。患者の50%が55歳までに最低1回の関節置換術を要する。小関節の症状は大きくない。
大量に排泄されるHGAの処理を行うのが腎臓であるため、腎機能障害が組織褐変と関節破壊を増悪させる[Introne et al 2002]。
他の臓器所見
心臓. 心臓弁や血管の色素沈着により動脈弁や僧帽弁の石灰化や閉鎖不全、ときに大動脈拡張が生じることがある。大動脈弁狭窄症は50歳~60歳代で多く発症する。一般集団の心臓弁疾患とは異なり、標準的な心血管リスク因子との相関がみられない。大動脈弁狭窄症は、時に大動脈弁置換術が必要となる。冠動脈の石灰化が胸部CTで確認されている[Hannoush et al 2012]。
腎臓結石. 64歳までに腎臓結石を発症するアルカプトン尿症患者は50%である。
腎臓はHGAを活発に分泌するため、アルカプトン尿症患者にとって腎機能は重要である。急性、慢性に関係なく腎損傷はHGAの排泄を妨げ、HGAが血液や組織に蓄積する原因となり、致命的なアシドーシス、溶血、メトヘモグロビン血症が生じる[Davison et al 2016, Freeman & Wills 2018, Hugar et al 2019]。
前立腺結石. 黒色の前立腺結石がアルカプトン尿症患者に比較的多く認められる。ある家系では、31~60歳の男性27名のうち8名が前立腺結石の既往があった。前立腺結石は再発性感染症や尿路閉塞の原因になりうるため、予防的手術が勧められる。
甲状腺. アルカプトン尿症では甲状腺機能低下症が高頻度に発現する。単一施設試験で、アルカプトン尿症の甲状腺機能低下症の頻度は16%であるのに対し、一般集団では3.7%であった[Avadhanula et al 2020]。
眼の組織褐変症. アルカプトン尿症患者1名において、眼の組織黒変が黒色肉腫と誤診され、眼球摘出された[Skinsnes 1948]。
遺伝型と臨床型の関連
HGD遺伝子変異の種類とHGA排泄量もしくは疾患の重症度との間に関連性は認められない。
アルカプトン尿症患者172名から同定したHGD病的バリアントの解析で、残存するHGD活性は1%未満~30%超であることが明らかになったが、血中HGA、尿中HGAおよび臨床的症状に差はみられなかった[Ascher et al 2019]。
病名
アルカプトン尿症は集合的に組織褐変症と呼ばれることがある(しかし、この名称は誤りである)。
頻度
1000人以上の罹患者について文献で報告されている。これはおそらく実際の患者数より少ない。米国におけるアルカプトン尿症の発症率は25万人に1人で、生産児では100万人に1人と推定されている。
アルカプトン尿症は世界中で発症している。
スロヴァキアにおけるアルカプトン尿症の有病率は推定19,000人中1人である[Zatkova et al 2003]。スロヴァキア北西で頻度が高いが、おそらく創始者変異の影響である。4つの病的バリアント(c.457dup,, c.481G>A,, c.808G>A, and c.1111dup)がスロヴァキアの創始者変異を代表しており、スロヴァキアの患者集団の病的バリアントの80%を占める(表 2参照)。
ドミニカ共和国では創始者変異(c.360T>G)の影響のため有病率が高い[Goicoechea De Jorge et al 2002]。
遺伝的に関連のある疾患
GeneReviewで説明されている以外で、HGD遺伝子の病的変異と関連する表現型は知られていない。
鑑別診断
組織褐変症. アルカプトン尿症による組織褐変は、慢性皮膚潰瘍の外用薬として用いられるフェノールの長期的使用後に生じる後天的可逆性色素変化と混同される場合がある[La Du 2001]。
抗マラリア薬のアタブリン(Atabrine®)[Ludwig et al 1963]、皮膚美白剤のハイドロキノン、抗生剤のミノサイクリンの長期使用後に化学的に誘発された組織褐変も報告されている[Suwannarat et al 2004, Stichman&West 2016]。
尿中HGAの過剰排泄が検出されない場合には徹底的な病歴聴取により偽陽性の診断を除外しなければならない。
関節炎. アルカプトン尿症の関節炎は、背骨と大関節を損傷する点で強直性脊髄炎に似ているが、仙腸関節が侵さないことと、X線画像で鑑別可能である。また、背骨のX線所見でリウマチ性関節炎および変形性関節炎とアルカプトン尿症を識別できる。
臨床的マネジメント
アルカプトン尿症の診療ガイドラインは公表されていない。
初回診断後の評価
アルカプトン尿症と診断された患者の疾患の程度と必要性において、要約した評価項目(診断の評価の一部として実行されていない場合)を推奨する:
- 注意深い病歴聴取と身体検査(とりわけ脊椎や大関節の可動域に注意を払うこと)
- 可動域が限られている場合、関節痛が生じた場合は理学療法やリハビリでの評価
- 40歳以上の患者に対する心電図および心エコー
- 腎臓の超音波検査や腹部ヘリカルCT画像検査による腎臓結石の有無の確認
- 原発性甲状腺機能低下症の評価のためのTSH濃度および遊離チロキシン濃度の測定
- 患者および患者家族にアルカプトン尿症の本質、遺伝方式、および遺伝的発症リスクを伝えるとともに、医学的決定および個人の意思決定を容易にするための遺伝医学者、認定遺伝カウンセラー、または遺伝看護専門看護師との相談
症状の治療
米国では、アルカプトン尿症の治療は対症療法である。欧州医薬品庁がアルカプトン尿症の治療薬としてニチシノンを承認しているが、これまで、米国医薬品局がアルカプトン尿症の治療薬としてニチシノンを承認したことはない。
対症療法
関節痛. アルカプトン尿症の関節痛は深刻であるため、注意深い疼痛管理が必要である。非ステロイド系抗炎症薬、神経痛の薬剤、アヘン薬といった多種多様な疼痛管理の選択肢を検討できる。代替えの疼痛管理として、理学療法、経皮電気的神経刺激術および神経ブロックも考慮できる。各患者の症状は異なり、投薬によっては禁忌であるかもしれない。綿密なフォローアップと長期的管理を行って、一人一人に合った適切な疼痛管理を行うこと。疼痛管理について、専門医との相談をすることも可能である。
筋力や柔軟性を適度に保つためには理学療法や作業療法が重要である。水泳のような適度な体重免荷運動による関節の可動域の維持がもたらす効果は大きい。
膝、腰、肩の関節置換術が重症な関節炎への1つの対処法となる。一般に、関節置換術の目的は可動域の増加というより疼痛緩和である。アルカプトン尿症患者では、変形性関節炎患者と比べ、関節置換術が人工関節置換術後の生存率(prosthetic survival)との関連性が高い。アルカプトン尿症の患者では、全関節置換術は関節の機能を手術前の状態より有意に改善する[Rajkumar et al 2020]。
大動脈狭窄は弁置換術が必要となる可能性がある。
前立腺結石および腎結石は外科的介入を必要とする可能性がある。
甲状腺機能低下は甲状腺刺激ホルモン補充療法が必要となる。
ニチシノン
4-ヒドロキシフェニルピルビン酸ジオキシゲナーゼ(HGAを生成する酵素)阻害剤であるニチシノンは、高チロシン血症I型の治療薬として米国および欧州で承認されている。
アルカプトン尿症を対象としたニチシノンの治験. 3年間の治験において、毎日2 mgのニチシノンを摂取すると、研究期間全体で尿中HGAおよび血中HGAが95%減少した[Introne et al 2011]。血漿チロシンは食事制限なしで平均800 μmol/L、およそ10倍上昇した。副作用は非常に少なかった。1名が角膜結晶を発症したため、ニチシノンを投与中止した。もう1名は肝トランスアミナーゼが上昇した。対照群と比較して、治療群では股関節可動域と筋骨格機能の測定値の統計的に有意な改善が認められなかったが、大動脈弁狭窄症の進行速度の低下には正の傾向があった(統計的に有意ではなかった)。
無作為化多施設共同追跡調査試験(ClinicalTrials.gov; NCT01916382)において、ニチシノン10 mg/日を投与したところ尿中HGA値が98%~99%減少した[Ranganath et al 2020]。本試験の主要評価項目は12ヵ月後時点の尿中HGA値の持続および血中HGA値の98%~99%減少であった。疾患の重症度の尺度として、Alkaptonuria Severity Score Indexを使用した。治療薬が投与されない対照群と比較し、ニチシノン投与群では疾患進行率が低下した。有害事象は血中チロシン濃度上昇による角膜症(13%)、原因不明の感染症増加であった。
無効な治療
無効な治療としては以下のようなものがある:
- HGAの産生量を低下させるためフェニルアラニンやチロシンの摂取制限が勧められるが、この2種類のアミノ酸の摂取を厳しく制限することは長期的にみて実際的でなく、危険性を伴うこともある。
- ビタミンCの大量摂取によりHGA誘導体の1つである尿中ベンゾキノン酢酸量が低下したが、HGAの排泄量には効果がなかった[Wolff et al 1989]。アスコルビン酸の大量摂取により黒色色素の沈着が予防できる可能性があるという仮説が提示されているが、基本的な代謝障害に変化をもたらすものではない[Wolff et al 1989]。アスコルビン酸の臨床的有効性を示した信頼できる研究はない[La Du 2001]。
経過観察
循環器. 40歳以降は心臓の合併症に対して1~2年に1回チェックを行うことが望ましい。大動脈拡張や大動脈弁や僧房弁の石灰化や閉鎖不全を検出するために心エコー検査を行うべきである。
冠動脈疾患の示唆的症状を有する場合、医師の推奨によりCT画像検査の対象となる場合がある。
泌尿器. 40歳以降は泌尿器合併症が多くみられるようになる。定期的な経過観察は推奨されないが、泌尿器の合併症が起こりうること自覚させるとよい。黒色化した前立腺結石がX線画像で認められることがある。また、腎臓結石は超音波検査や腹部ヘリカルCT画像で検出できる。
甲状腺。 最初の診断時に甲状腺機能を評価し(TSHおよび遊離サイロキシン)、その後1~2年毎に原発性甲状腺機能低下症を評価する。
回避すべき薬物や環境
脊椎や大関節への物理的負荷を避ける(重労働や衝撃の大きいスポーツ)。これにより重症関節炎への進行を遅らせることができるかもしれない。
若年患者には衝撃の強いスポーツや接触の多いスポーツを避けるよう指導する。
リスクのある親族への評価
予防措置の恩恵を受ける人をできるだけ早く特定するために、一見無症状の同胞を評価することは適切である。評価には以下が含まれる:
- 尿中HGA値の上昇に対する生化学検査
- 家族内でHGD病的バリアントが同定されている場合、分子遺伝学的検査
アルカプトン尿症の患者には衝撃の強いスポーツや接触の多いスポーツを避けるよう指導する。職業選択の際には、重労働を含む職業を避けることも考慮する。適切な運動とともに関節を強化し柔軟性を高める運動を行うことで、全般的な関節の可動性と機能を維持に役立つ可能性がある。
遺伝カウンセリングとして扱われるリスクのある親族への検査に関する問題は「遺伝カウンセリング」の項を参照のこと。
研究中の治療法
種々の疾患に対する臨床試験については,ClinicalTrials.govおよびEU Clinical Trials Registerを参照のこと。
注:本症の臨床試験が行われていない可能性がある。
遺伝カウンセリング
「遺伝カウンセリングは個人や家族に対して遺伝性疾患の本質,遺伝,健康上の影響などの情報を提供し,彼らが医療上あるいは個人的な決断を下すのを援助するプロセスである.以下の項目では遺伝的なリスク評価や家族の遺伝学的状況を明らかにするための家族歴の評価,遺伝学的検査について論じる.この項は個々の当事者が直面しうる個人的あるいは文化的、倫理的な問題に言及しようと意図するものではないし,遺伝専門家へのコンサルトの代用となるものでもない.」
遺伝形式
アルカプトン尿症は常染色体潜性遺伝(劣性遺伝)性疾患である。
注: 信頼できる再発リスク評価を家族に提供するために、アルカプトン尿症の分子診断は発端者(すなわち、両親HGD病原性バリアントを同定)で確立されなければならない。
家族構成員のリスク
発端者の両親
- ヘテロ接合体(保因者)は無症状である(家族歴に基づき、一つのHGD病的バリアントの保因者と推測される)。
- 発端者の両親にアルカプトン尿症の分子遺伝学的診断を実施して、HGD病的バリアントのヘテロ接合体であることを確認し、信頼できる再発リスク評価を家族に提供することが推奨される。片方の親からのみ病的バリアントが同定された場合、以下の可能性を検討すべきである:
- 発端者で同定された病原性バリアントが、発端者におけるde novoとして現れた、またはモザイクを有する親における後天性de novoとして現れた[Jónsson et al 2017]。
- 病原性バリアントを有する片方の親の染色体の片親性ダイソミーによって、発端者の病原性バリアントのホモ接合性が生じた。
- ヘテロ接合体(保因者)は無症状でアルカプトン尿症の発症リスクがない。
発端者の同胞
- 両親がHGD病原性バリアントについてヘテロ接合であることが判明している場合、患者の同胞は受胎時に25%の確率で罹患し、50%の確率で無症候性の保因者であり、25%の確率で無症状かつ保因者でもない。
- ホモゲンチジン酸の尿中排泄と疾患の重症度は、同じHGD病原性バリアントを有する同胞間で大きく異なる可能性がある。
- ヘテロ接合体は無症状でアルカプトン尿症の発症のリスクを有しない。
発端者の子
アルカプトン尿症患者の子は必ずヘテロ接合体(保因者)であり、HGDに病的バリアントを有する。
他の家族構成員
発端者の同胞は50%の確率でHGDに病的バリアントの保因者である。
保因者の検出
分子遺伝学的検査。 発症リスクを有する血縁者の保因者診断は、家系内のHGD病的バリアントが同定されていれば可能である。
生化学検査。 生化学的検査による遺伝子検査は保因者診断の方法としては信頼性がない
遺伝カウンセリングに関連した問題
早期診断や早期治療目的の発症リスクを有する血縁者への検査に関する情報は、「臨床的マネジメント」、「発症リスクのある血縁者への検査」の項を参照のこと。
家族計画
- 遺伝リスクの決定や出生前/着床前診断の利用について話し合う最適な時期は妊娠前である。
- 罹患している若年成人やリスクのある若年成人に対して遺伝カウンセリング(子への潜在的リスクや生殖手段)の提供は適している。
出生前/着床前遺伝子診断
分子遺伝学的検査。家族内にHGD 病的バリアントが同定された場合、リスクのある妊娠に対する出生前検査およびアルカプトン尿症に対する着床前遺伝子検査が可能な場合がある。
出生前診断については、専門医の間でも家族によっても考え方が異なるだろう。たいていの医療機関では出生前診断を受けるかどうかの決定は両親の選択に委ねると考えるであろうが、この問題に関しては慎重な議論が必要である。
分子遺伝学
分子遺伝学とOMIMの表の情報はGeneReviewsの他の場所の情報とは異なるかもしれない。表は、より最新の情報を含むことがある。
表A. アルカプトン尿症: 遺伝子とデータベース
| 遺伝子 | 染色体遺伝子座 | タンパク質 | 遺伝子座固有のデータベース | HGMD | ClinVar |
|---|---|---|---|---|---|
| HGD | 3q13.33 | ホモゲンチジン酸1,2-ジオキシゲナーゼ | AKUデータベース HGD変異のデータベース HGDのデータベース |
HGD | HGD |
データは、HGNCの遺伝子、OMIMの染色体座、UniProtのタンパク質という標準的なレファレンスから編集されている。リンク先のデータベース(Locus Specific、HGMD、ClinVar)については、こちらを参照する。
表B. アルカプトン尿症のOMIMエントリー(OMIMですべて見る)
| 203500 | アルカプトン尿症; AKU |
| 607474 | ホモゲンチジン酸1,2-ジオキシゲナーゼ; HGD |
更新履歴:
-
Gene Reviews著者: Wendy J Introne, MD, Michael A Kayser, DO, William A Gahl, MD, PhD
日本語訳者: 窪田美穂(ボランティア翻訳者),鳴海洋子(信州大学医学部附属病院遺伝子診療部)
Gene Reviews 最終更新日: 2011.3.10.日本語訳最終更新日: 2011.4.1 - Gene Reviews著者: Wendy J Introne, MD, Michael A Kayser, DO, William A Gahl, MD, PhD
日本語訳者: 吉村祐実(ボランティア翻訳者),櫻井晃洋(札幌医科大学附属病院遺伝子診療科)
GeneReviews最終更新日:2021.6.10. 日本語訳最終更新日: 2022.8.25.[ in present]
原文 Alkaptonuria