遺伝性乳がん/卵巣がん
(BRCA1 and BRCA2 Hereditary Breast/Ovarian Cancer)
[HBOC]
Gene Review著者: Nancie Petrucelli, MS, Mary B Daly, MD, PhD, Gerald L Feldman, MD, PhD, FACMG.
日本語訳者: 窪田美穂(ボランティア翻訳者),櫻井晃洋(信州大学医学部附属病院遺伝子診療部)
Gene Review 最終更新日: 2011.1.20. 日本語訳最終更新日: 2011.3.20.
原文 BRCA1 and BRCA2 Hereditary Breast/Ovarian Cancer
要約
疾患の特徴
BRCA1遺伝子もしくはBRCA2遺伝子の生殖細胞系列変異により,乳がんおよび卵巣がん,その他のがんの易罹患性が生じる.BRCA1遺伝子もしくはBRCA2遺伝子の生殖細胞系変異関連の腫瘍発症リスクを罹患者が複数いる家系,罹患者が少数である家系,および民族ベースの研究から求めると,家系ごとにバラツキが認められるようである.乳がんや卵巣がんの生命予後はがん診断時の病期によって決まるが,生存に関する試験で対照群と比較した場合,BRCA1遺伝子やBRCA2遺伝子の生殖細胞系変異を有する患者に関する結果は試験ごとに相反している.
診断・検査
BRCA1遺伝子およびBRCA2遺伝子の生殖細胞系変異に対する分子遺伝学的検査は,患者の既往や家族歴からみて発症リスクが高い場合,またBRCA1遺伝子もしくはBRCA2遺伝子に生殖細胞系変異を有する患者の血縁者であるため発症リスクの高いとされる場合には,臨床的に利用可能である.今のところBRCA1遺伝子もしくはBRCA2遺伝子におけるがん易罹患性変異をすべて同定すると保証されている技術は存在しない.また,臨床的意義が不明の変異が同定される場合もある.
臨床的マネジメント
病変の治療: BRCA1遺伝子もしくはBRCA2遺伝子関連の腫瘍をもつ患者に対する乳がんと卵巣がんの治療は,これらのがんの孤発例に対する治療と同じであるが,BRCA1/2シグナル伝達経路を特異的標的とする新しい薬効群が試験中である.
一次病変の予防: 予防的乳房切除術や卵巣摘出術,タモキシフェン(部分的エストロゲン拮抗薬)を用いた化学予防が行われているが,高リスク女性に対するランダム化試験や症例対照研究による評価はまだ行われていない.
定期検査: 推奨されているがんのスクリーニング検査は家系内でもっとも早期に発症した人の年齢によって調整する必要があるが,ランダム化試験や症例対照研究による評価が行われていない.乳がんのスクリーニング検査は男女とも毎月の乳房の自己チェック,毎年または半年ごとの病院での乳房触診,毎年のマンモグラフィー,そしてMRI撮影を組み合わせて行う.卵巣がんのスクリーニング検査は,毎年または半年ごとの骨盤部診察,毎年または半年ごとのカラードプラー法を併用した経膣超音波検査,および毎年の血清CA-125値の測定を組み合わせて行う.前立腺がんのスクリーニング検査では毎年の直腸診と前立腺特異抗原(PSA)検査を行う.
リスクのある血縁者の検査: 患者にBRCA1遺伝子もしくはBRCA2遺伝子の生殖細胞系変異が同定された場合,発症リスクのある血縁者に検査を行うことにより家系特異的な変異を有する血縁者を同定することができるため,その血縁者は定期検査を受け,がんが見つかった場合には早期治療が可能となる.遺伝カウンセリング
BRCA1遺伝子やBRCA2遺伝子の生殖細胞系変異の遺伝形式は常染色体優性である.BRCA1遺伝子やBRCA2遺伝子の生殖細胞系変異を有する人の子が変異を受け継ぐ確率は50%である.家系特異的な変異が同定されている場合には,BRCA1遺伝子やBRCA2遺伝子の生殖細胞系変異を受け継ぐリスクのある無症状の血縁者に対して分子遺伝学的検査を行うことができる.家系内のがん易罹患性変異が同定されている場合にはリスクの高い妊娠に対する出生前診断が可能だが,成人発症疾患に対する出生前診断の希望は少なく,また注意深い遺伝カウンセリングが必要である.
診断
臨床診断
家系内に以下の項目のうち最低1項目が該当する場合,BRCA1遺伝子やBRCA2遺伝子の生殖細胞系変異による遺伝性乳がん・卵巣がんが疑われるため,さらなるリスク評価が必要となる[National Comprehensive Cancer Network 2010]:
- 若年発症性(発症年齢50歳未満)の乳がん(浸潤性乳がんや非浸潤性乳管がん(DCIS))
- 1人の患者に原発性乳がんが2カ所,もしくは乳がんや卵巣・卵管・原発性腹膜がんが2カ所認められる場合,または父方もしくは母方の家系内の近親(1度〜3度近親)に2カ所以上の原発性乳がん,もしくは乳がんや卵巣・卵管・原発性腹膜がんが2カ所以上認められる場合
- 発症リスクのある民族集団(アシュケナージ系ユダヤ人など)
- BRCA1遺伝子やBRCA2遺伝子の変異を有することがわかっている家系の血縁者
- 男性乳がん患者
- 発症年齢を問わず,卵巣・卵管・原発性腹膜がんの罹患
以下の状況では,遺伝性乳がん・卵巣がんの疑いが強まる:
- 家族構造が限られている家系,すなわち,父方,母方のどちらかで,1度近親もしくは2度近親で45歳まで生存した女性が2人未満の場合,易罹患性の家系内変異があるにもかかわらず,女性がんの存在が低く見積もられているのかもしれない.
- 血縁者の若年での卵巣摘出術.卵巣摘出術により乳がんと卵巣がんのリスクはともに減少するため,乳がんと卵巣がんへの遺伝的な易罹患性を覆い隠している可能性がある.
- 家系で養子縁組が存在する場合
- BRCA1遺伝子もしくはBRCA2遺伝子の変異を有するリスクのある民族(アシュケナージ系ユダヤ人の子孫など)
1個人もしくは1家系がBRCA1遺伝子やBRCA2遺伝子に変異を有する確率を推測する確率モデルが開発された.それぞれのモデルにはモデル作成に用いられた方法や症例数,人口集団に由来する独自の特徴がある.汎用されているこのようなモデルの2つがBRCAPROとMyriad IIである(表1で両者の比較を行った).
- BRCAPRO[Parmigiani et al 1998]はコンピュータに基づいたベイズ流確率モデルであり,1度近親および2度近親の乳がんや卵巣がんの家族歴を用いて,家系内での乳がんや卵巣がんの発症パターンをBRCA1遺伝子もしくはBRCA2遺伝子の変異で説明しうる確率を求める.重要な属性には集団における変異頻度,年齢特異的浸透度,アシュケナージ系ユダヤ人の子孫であるかなどが含まれる.BRCAPROはCancerGeneソフトウェアの一部として利用できる.注:BRCAPROモデルは頻繁に改訂されるため,この記述が行われた日時の状況は現在の状況とは異なる.
- Myriad IIは患者や1度近親もしくは2度近親の民族的出自(アシュケナージ系ユダヤ人か非アシュケナージ系ユダヤ人),乳がん発症年齢(50歳未満か50歳以上),卵巣がんの有無により分類した一群の頻度表である.Myriad IIはMyriad Genetic Laboratories社が行っている実際の臨床検査データに基づく[Frank et al 2002].オンライン版の頻度表は頻繁に改訂される.
- その他,それほど用いられていない確率モデルにManchester Scoring System,Breast and Ovarian Analysis of Disease Incidence,Carrier Estimation Algorithm (BOADICEA)(TM),Tyrer-Cuzickがある[Antoniou et al 2004, Evans et al 2004, Tyrer et al 2004].
表1.BRCAPROモデルおよびMyriad II変異頻度表:長所と限界
|
BRCAPROモデル |
Myriad II変異頻度表 |
長所 |
|
|
|
・広範な家族歴情報が必要でない | |
限界 |
|
● 家系情報は記入用紙の記載によるので限界がある |
1. テキサス大学ダラス・サザンウェスタン医学センターにより開発された
分子遺伝学的検査
GeneReviewsは,分子遺伝学的検査について,その検査が米国CLIAの承認を受けた研究機関もしくは米国以外の臨床研究機関によってGeneTests Laboratory Directoryに掲載されている場合に限り,臨床的に実施可能であるとする. GeneTestsは研究機関から提出された情報を検証しないし,研究機関の承認状態もしくは実施結果を保証しない.情報を検証するためには,医師は直接それぞれの研究機関と連絡をとらなければならない.―編集者注.
遺伝子 BRCA1遺伝子とBRCA2遺伝子は遺伝性乳がん・卵巣がんに関連する2つの遺伝子である.
臨床検査
- 標的変異解析.標的変異解析は集団特異的なものであり,特定の民族的背景を持つ人に高頻度に同定される変異を対象とする(図1参照).
- シークエンス解析.その他の方法と併用してシークエンス解析を行うことにより,BRCA1遺伝子やBRCA2遺伝子に多くみられる変異や家系特異的変異を検出できる.アシュケナージ系ユダヤ人家系を除き,家系内変異が不明な場合にはシークエンス解析や変異スキャニング法が推奨される(「検査手順」,「アシュケナージ系ユダヤ人の発端者」の項を参照のこと).1つのエクソンが欠失していたり,数百もしくは数千の塩基が欠失していたり,また新たな配列が挿入されていたりする複雑なBRCA1アレルもしくはBRCA2アレルを検出する際には,シークエンス解析と欠失解析の両方が必要とされる(表Aを参照のこと).
- 欠失・重複解析.さまざまな方法がゲノム構造の異常(大規模な欠失,重複,再構成など)の解析に用いられる.
図1.アシュケナージ系ユダヤ人におけるBRCA1遺伝子およびBRCA2遺伝子変異
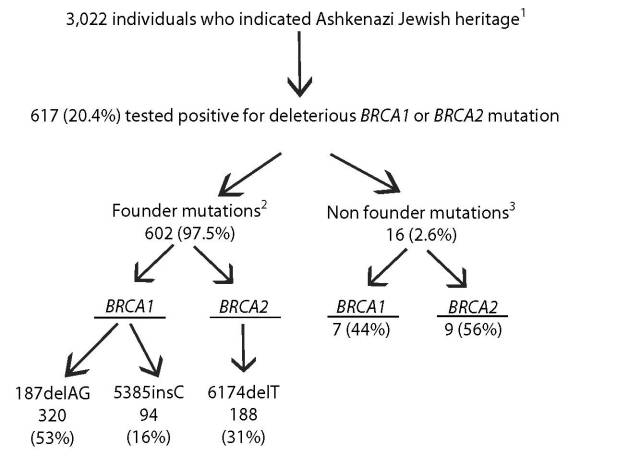
- Frank et al [2002]
- 標的変異解析により検出(表4,5を参照のこと)
- シークエンス解析のみにより検出
表2.遺伝性乳がん・卵巣がんにおける分子遺伝学的検査
当該遺伝子変異による遺伝性乳がん・卵巣がんの割合 |
検査方法 |
検出変異 |
検査の利用 |
|
BRCA1 |
図1,図2を参照のこと |
標的変異解析 |
民族特異的 |
|
シークエンス解析 |
シークエンス・バリアント 1 |
|||
欠失・重複解析2 |
1つのエクソンもしくは複数のエクソンの欠失;複雑アレル |
|||
BRCA2 |
標的変異解析 |
民族特異的 |
||
シークエンス解析 |
シークエンス・バリアント 1 |
|||
欠失・重複解析2 |
1つのエクソンもしくは複数のエクソンの欠失;複雑アレル |
GeneReviewsは,分子遺伝学的検査について,その検査が米国CLIAの承認を受けた研究機関もしくは米国以外の臨床研究機関によってGeneTests Laboratory Directoryに掲載されている場合に限り,臨床的に実施可能としている.GeneTestsは研究機関から提出された情報の検証や,研究機関の承認状態もしくは実施結果の保証は行わない.情報を検証するためには,医師は直接それぞれの研究機関と連絡をとらなければならない.
-
シークエンス解析で検出される変異には,小規模な遺伝子内欠失・挿入,ミスセンス変異,ナンセンス変異,スプライス部位の変異などがある.
-
ゲノムDNAのシークエンス解析で容易に検出できない欠失・重複を同定する検査には,定量PCR法,ロング・レンジPCR法,MLPA法,(遺伝子・セグメント特異的)標的アレイGH法といったさまざまな方法がある.ゲノム全般の欠失・重複を検出する全領域アレイGH解析もこの遺伝子・セグメントに含まれる.「アレイGH法」を参照のこと.
発端者の検査結果の解釈
標的変異解析.アシュケナージ系ユダヤ人に多く見られる3種類の変異を検査した際に発端者に生じうる検査結果:
-
変異なし. この検査はアシュケナージ系ユダヤ人に関連する3種類の創始者変異(c.68_69delAG [BRCA1]変異,c.5266dupC [BRCA1]変異,c.5946delT [BRCA2]変異 )(図1,図2,表4,表5を参照)のみを検出するものであるため,変異を検出できない(検査結果「陰性」)からといってその患者がBRCA1遺伝子やBRCA2遺伝子に別の易罹患性の生殖細胞系変異がないということにはならない.アシュケナージ系ユダヤ人に対しては,この民族に多い3種類の遺伝子変異が1つも検出されない場合,その後にシークエンス解析や重複・欠失解析を勧めるかどうかは臨床判断,生殖細胞系変異を有する事前のリスク,これ以外のBRCA1遺伝子やBRCA2遺伝子の生殖細胞系変異(上記3種類以外の多くみられる変異)が存在するリスクによって決められる.しかし,これまで発症リスクの高いアシュケナージ系ユダヤ人で大規模な再構成は同定されていないため[Spence et al 2007, Stadler et al 2010],このような患者に対する欠失・重複解析の実施は非常に限られたものとなるだろう .
- 変異あり. 生殖細胞系変異が認められる場合(検査結果「陽性」),BRCA1遺伝子もしくはBRCA2遺伝子関連のがん発症リスクが高いことを意味している.とりわけ父方,母方双方がアシュケナージ系ユダヤ人である場合には,発症リスクのある血縁者へのフォローアップ検査の実施が推奨される.幾つかのアシュケナージ系ユダヤ人家系で複数の生殖細胞系の創始者変異が同時に存在していたことが報告されているため,発端者で認められた変異がなんであろうと,アシュケナージ系ユダヤ人に多い3種類の変異すべてに対する標的変異解析も行う[Ramus et al 2001].
- 結果が不確実な場合. 使用する検査方法を考慮すると,BRCA1遺伝子もしくはBRCA2遺伝子のアシュケナージ系ユダヤ人に多い3種類の変異の1つに隣接して,新しく臨床的意義が不明のバリアントが検出される可能性がある.標的変異解析は遺伝子の小さな部分に絞って行われるため,このようなことが稀に起こる.一般にこれは1塩基置換であり,タンパク質の機能に影響を与える場合と与えない場合がある.このような結果をさらに評価するため,検査機関が家系内のがんと家系内の別の血縁者(通常,罹患者もしくは被検者の両親)の血液検体を求め,このバリアントが家系内のがんと共分離するかを確定することがある.このような検査により当該バリアントが発症に関与しているのか,もしくは臨床的意義のない正常な多型であるかが明らかにされるであろう.
シークエンス解析. 発端者に生じうる検査結果:
- 変異なし 発端者で生殖細胞系変異が検出されない場合,得られる情報は限られている.家系の発癌原因が確立されないことから解釈は慎重に行わなければならない.その他の可能性もある:家系内のがんは(a)シークエンス解析で検出できないBRCA1遺伝子もしくはBRCA2遺伝子の生殖細胞系変異に関連している,(b)別のがん感受性遺伝子の変化が原因である,もしくは(c)非遺伝的要因による発症である.したがって,BRCA1遺伝子もしくはBRCA2遺伝子の生殖細胞系変異が検出されないからといって,当該家系における遺伝性のがん易罹患性の可能性がなくなったわけでないことに注意すべきである.シークエンス解析結果の解釈に際して考慮すべきその他の事柄に関しては,こちらをご覧ください.
- 変異あり 発端者がBRCA1遺伝子もしくはBRCA2遺伝子に生殖細胞系変異を有する場合,BRCA1遺伝子もしくはBRCA2遺伝子関連のがん発症リスクが高いことを意味する.
- 結果が不確実な場合. シークエンス解析によりBRCA1遺伝子やBRCA2遺伝子のいずれにも臨床的意義が不明のDNAバリアントが発見されることがある.バリアントががんの表現型を決定しているかを確認する試みの一つとして家系調査が開始されることがある.BRCA1遺伝子およびBRCA2遺伝子変異に対する遺伝子検査を受けた者の10〜15%に臨床的意義が不明のバリアントが認められることが示されている[Frank et al 2002].
欠失・重複解析. シークエンス解析後,変異が1つも検出されなかったり検査結果が不確実だった場合,BRCA1遺伝子やBRCA2遺伝子の欠失や複雑アレルに対する検査が考慮されることがある.欠失・重複解析では以下の結果が生じうる.
- 欠失・重複なし. 欠失・重複が検出されない場合(検査結果「陰性」),家系内のがんの発症原因が確立していないため,解釈を慎重に行わなくてはならない.その他の可能性もある:家系内のがんは(a)欠失・重複解析で検出できない変異に関連している,(b)別のがん感受性遺伝子における変化が原因である,もしくは(c)非遺伝的要因による発症である.したがって,BRCA1遺伝子もしくは欠失(もしくは複雑アレル)が検出されないからといって,当該家系における遺伝性のがん易罹患性の可能性がなくなったわけでないことに注意すべきである.
- 欠失・重複あり.BRCA1遺伝子もしくはBRCA2遺伝子の生殖細胞系の欠失・重複が認められる場合(検査結果「陽性」),BRCA1遺伝子もしくはBRCA2遺伝子関連のがん発症リスクが高いことを意味する.
リスクのある血縁者の検査結果の解釈
家系特異的変異.罹患者家系に存在することがわかっている生殖細胞系変異を有するリスクのある血縁者の検査から生じうる検査結果:
- 変異なし.変異が検出されない場合(検査結果「陰性」),被検者は家系特異的変異を受け継いでおらず,BRCA1遺伝子もしくはBRCA2遺伝子関連のがん発症リスクはすくなくとも一般集団と同等である.
- 変異あり.生殖細胞系変異が認められる場合(検査結果「陽性」),被検者は家系特異的変異を受け継いでおり,BRCA1遺伝子もしくはBRCA2遺伝子関連のがん発症リスクが高い
検査手順
アシュケナージ系ユダヤ人の発端者
標的変異解析.アシュケナージ系ユダヤ人では,3種類の生殖細胞系変異(c.68_69delAG (BRCA1)変異,c.5266dupC (BRCA1)変異,c.5946delT (BRCA2)変異)が観察されている.アシュケナージ系ユダヤ人では40人に1人という高率でこれらの3種類の創始者変異が認められる[Struewing et al 1997].したがって,アシュケナージ系ユダヤ人に対する検査では,BRCA1遺伝子もしくはBRCA2遺伝子の生殖細胞系変異の有無を確認する際,最初にシークエンス解析を行うというその他の民族で推奨されるやり方よりも,まずこれらの3種類の創始者変異に対する標的変異解析を行うことが効率的な評価方法である.
シークエンス解析.標的変異解析で変異が同定されない場合,次にシークエンス解析を行うことが妥当であろう.この決定は当該被検者に対する臨床判断,事前の変異リスク,この3種類以外にBRCA1遺伝子もしくはBRCA2遺伝子の生殖細胞系変異を有するリスクに基づく.
欠失・重複解析. これまで高リスクのアシュケナージ系ユダヤ人では1つのエクソンもしくは複数のエクソンの欠失は検出されていないため[Spence et al 2007, Stadler et al 2010],この集団では欠失・重複解析を用いた検査が必要でないことがある.
BRCA1遺伝子もしくはBRCA2遺伝子の生殖細胞系変異を持つかどうかが不明な家系
初めに検査を受ける者がすでに乳がんや卵巣がんを発症している場合,とりわけ乳がんの発症が通常より若年である場合(50歳未満)には,血縁者に対する生殖細胞系変異の検査から多くの情報が得られることが多い.このため,BRCA1遺伝子もしくはBRCA2遺伝子の生殖細胞系変異を有すると可能性が高い血縁者や,非遺伝性の乳がんもしくは卵巣がんを発症している可能性が低いと考えられる血縁者に対しては,可能な場合はいつでも分子遺伝学的検査を実施すること.
罹患している血縁者が死亡した場合,もしくは分子遺伝学的検査を受けたがらない場合や受けることができない場合,変異が検出されなくても家系内のBRCA1遺伝子やBRCA2遺伝子の生殖細胞系変異が存在する可能性がなくなったわけではないことを考慮して,がんの既往がない者に対してシークエンス解析を用いた生殖細胞系変異に対する検査(必要な場合には,その後の欠失・重複解析)を実施する.
BRCA1遺伝子もしくはBRCA2遺伝子の生殖細胞系変異を有することがわかっている家系におけるリスクのある無症状の成人血縁者に対する発症前診断. 生殖細胞系変異が家系内に同定された場合,成人血縁者(がんの既往がない血縁者を含む)が同一の家系特異的生殖細胞系変異を有するかどうかを高い精度で検査できる.大多数の場合,発症リスクのある血縁者は家系特異的な生殖細胞系変異のみを検査すればよい.しかし,この例外として以下が挙げられる:
アシュケナージ系ユダヤ人に対しては,複数の生殖細胞系の創始者変異が共存する家系が幾つか報告されているため,3種類の生殖細胞系の創始者変異がすべて検査すること.
父方と母方の双方にBRCA1遺伝子もしくはBRCA2遺伝子の生殖細胞系変異を有する可能性のある場合,例えば,母方に生殖細胞系変異が同定されていると同時に父方でも遺伝性乳がん・卵巣がんが疑われる場合にはシークエンス解析を行い,その後にBRCA1遺伝子およびBRCA2遺伝子に対する欠失・重複解析を受けることが推奨される.これにより,(1)母方の家系の生殖細胞系変異が存在すれば検出されると同時に,(2)父方にも生殖細胞系変異が追跡できるか確かめることができるだろう.
リスクのある妊娠に対する出生前診断や着床前診断(PGD)には家系内のBRCA1遺伝子もしくはBRCA2遺伝子の生殖細胞系変異の事前同定が必要である.
注:GeneTests Laboratory Directoryの掲載施設で実施可能な臨床検査を載せることがGeneReviewsの方針である.ここで掲載されている検査は必ずしも著者や編集者や審査者の推奨を反映するものではない.
遺伝的に関連のある疾患
BRCA2遺伝子の生殖細胞系変異は以下の疾患と関連がある:
- 家族性膵がん[Naderi & Couch 2002, Hahn et al 2003]
- ファンコニ貧血相補群FANCD1[Howlett et al 2002]
臨床像所見
自然経過
乳がんの予後. BRCA1遺伝子関連腫瘍(おそらくBRCA2遺伝子関連腫瘍も同様)の病理的特徴は,乳がんの家族歴をもたない乳がん患者でBRCA1遺伝子やBRCA2遺伝子の体細胞系変異があまりみられないことも併せて考えると,がん易罹患性をもつBRCA1遺伝子やBRCA2遺伝子の生殖細胞系変異には特殊な発症要因があり,このために予後に違いが生じていると考えられる.BRCA1遺伝子やBRCA2遺伝子のがん易罹患性の生殖細胞系変異を有する患者における乳がんの予後を正確に評価するには,多数の女性の長期にわたる前向き研究が必要である.このような研究はまだ報告されていない.
現在得られているデータの多くは間接的もしくは後ろ向き研究によるものであり,症例数も少なく(50例未満),おそらくさまざまなバイアスや適切な比較対照群の欠落のために混乱したものとなっている(対照群は,診断時の年齢やがんの病期分類だけでなく,近年の生存率の改善を考えると診断の暦年も一致させなければならない).たとえば,乳がんの予後に関するほとんどの研究で対照群に対する分子遺伝学的検査は実施されておらず,対照群の診断時の病期も一致していない.一部の研究者は診断時の病期を一致させると,たとえば,がん易罹患性の生殖細胞系遺伝子変異を有する者にでの最初のがんの検出がより進行した病期でなされる場合など,BRCA1・BRCA2関連腫瘍と非遺伝性腫瘍の真の生物学的差異が見えにくくなるかもしれないと主張している.しかし,この主張にはまず,BRCA1遺伝子もしくはBRCA2遺伝子にがん易罹患性の生殖細胞系変異を有する女性と非遺伝性腫瘍を有する女性の診断時の病期が実際に異なっているという(現在のところ欠けている)確固たる証拠が必要であろう[Pharoah et al 1999].
こうした限界もあり,ほとんどの乳がんの予後に関する研究でがん易罹患性のBRCA1遺伝子もしくはBRCA2遺伝子の生殖細胞系変異を有する群と対照群との間に有意な差が認められていないが[Gaffney et al 1998, Johannsson et al 1998, Verhoog et al 1998, Lee et al 1999, Verhoog et al 1999, Brekelmans et al 2007, Rennert et al 2007, Budroni et al 2009, Kriege et al 2009],予後がより良いとする報告[Porter et al 1994, Marcus et al 1996]と悪いとする報告[Foulkes et al 1997, Ansquer et al 1998, Stoppa-Lyonnet et al 2000, Brekelmans et al 2006]がある.
アシュケナージ系の乳がん家系に対する後ろ向きコホート研究では,アジュバント化学療法を受けていない女性に限って言えば,BRCA1遺伝子の生殖細胞系変異を有する者はBRCA1遺伝子の生殖細胞系変異をもたない対照群と比較して,疾患特異的な生存率が低かった[Robson et al 2004].幾つかの研究報告では,保存的治療を受けた女性で対側乳がん[Robson et al 1999, Stoppa-Lyonnet et al 2000, Haffty et al 2002, Brekelmans et al 2006]および同側乳がん[Robson et al 1999, Haffty et al 2002, Seynaeve et al 2004]の発症率が高かった.ある症例対照研究では,予防的卵巣摘出術を受けていないBRCA1遺伝子もしくはBRCA2遺伝子の生殖細胞系変異を有する者だけに同側乳がんの発症率が高かった[Pierce et al 2006].こうした研究で報告されている第2の原発性がんの増加は,顕著な生存率の差につながっていない.
卵巣がんの予後. がん易罹患性のBRCA1遺伝子とBRCA2遺伝子の生殖細胞系変異を有する女性における卵巣がんの生存率の研究では結果が交錯しており,その理由の1つは乳がんの予後研究でみられたのと同じ方法論的問題による.
スウェーデン(症例数38)やカナダ(症例数44)における地域住民調査研究では,がん易罹患性のBRCA1遺伝子の生殖細胞系変異群と対照群との間に生存率の差は認められなかった[Brunet et al 1997, Johannsson et al 1998].オランダでの症例対照研究では短期間の予後改善が認められたが,5年後には消失していた[Zweemer et al 2001].アイオワ大学で行なわれた症例対照研究でも,BRCA1遺伝子変異が不活化された女性における予後の方が良好であるという結果は得られなかった[Buller et al 2002].
英国における小規模な症例対照研究では,BRCA遺伝子変異陽性患者における完全奏効率(81.8%対43.2%;p=.004)および全生存率(95.5%対59.1%;p=.002)はどちらも高かった[Tan et al 2008].全国イスラエル卵巣がん調査の報告では,アシュケナージ系創始者変異を有する者は持たない者と比較して,生存期間の中央値(53.7カ月対37.5カ月;p=.002)および5年生存率(38.1%対24.5%;p=<0.001)が著しく良好であった[Chetrit et al 2008].2件の地域住民調査研究では,BRCA2遺伝子変異陽性者はBRCA1変異陽性者と比べて生命予後が良好であると報告された[Pal et al 2007, Byrd et al 2008].
したがって,がん易罹患性のBRCA1遺伝子もしくはBRCA2遺伝子の生殖細胞系変異を有する卵巣がん患者における相対的な予後は不明であるが,BRCA1遺伝子変異細胞で白金製剤への感受性が高いことを示す実験データは,白金製剤治療を受けた女性の予後が良好であることの生物学的根拠となっている[Lafarge et al 2001, Quinn et al 2003].
病理
乳がんの病理. BRCA1遺伝子関連腫瘍では髄様腺管がんが多く,組織学的異型度が高く,非遺伝性腫瘍と比べてエストロゲン受容体陰性およびプロゲステロン受容体陰性であることが多く,HER2/neuの過剰発現の頻度は低い.したがって,BRCA1遺伝子関連腫瘍は「トリプルネガティブ」乳がんの部類に入る[Rakha et al 2008].分子レベルでは,BRCA1遺伝子関連腫瘍では非遺伝性腫瘍よりもTP53変異の頻度が高い.これらの特徴は予後因子として好ましい場合もあれば好ましくない場合もある.
集積しつつあるデータから,BRCA1遺伝子関連の乳がんは非遺伝性腫瘍と比べて乳腺の表皮基底層細胞に由来することが多いことがわかっている.乳腺の表皮基底層細胞は乳腺幹細胞の役割を果たしていると考えられており,BRCA1遺伝子関連腫瘍で見られる異型度の高いがんの発生母体となると考えられている[Foulkes et al 2003, Foulkes et al 2004, Lacroix & Leclercq 2005, Lakhani et al 2005, Atchley et al 2008].
BRCA2遺伝子関連腫瘍に関する情報はずっと限られたものであるが,特徴的な組織像はないようであり,すくなくともホルモン受容体陽性の頻度は対照群の腫瘍と同程度である.
卵巣がんの病理. がん易罹患性のBRCA1遺伝子もしくはBRCA2遺伝子の生殖細胞系変異を有する女性では,対照群と比べて漿液性腺がんがきわめて多い.がん易罹患性のBRCA1遺伝子の生殖細胞系変異を有する女性では腫瘍の90%以上が漿液性であるが,がん易罹患性のBRCA1遺伝子の生殖細胞系変異を持たない女性では約50%である[Rubin et al 1996, Aida et al 1998, Berchuck et al 1998, Lu et al 1999].漿液性腺がんは粘液性がんに比べて,一般に異型度が高く,両側性であることが多い.
予防的卵巣摘出術の際に切除した卵管に対する注意深い組織病理学的解析から,原発性卵管がんと卵管上皮内がんの潜在的発症部位として卵管采が同定された.また,このような卵管がんの多くでは漿液性がんで過剰蓄積されるp53タンパク質が染色される[Crum et al 2007].このような所見から,原発性卵管がんに加えて卵管采も幾つかの腹膜がんや漿液性卵巣がんの起源となっている可能性が示唆される[Carlson et al 2008].
DNAマイクロアレイ技術を用いて,非遺伝性卵巣がんとBRCA1・BRCA2遺伝子関連の卵巣がんにおける遺伝子発現の違いを比較した際に得られた所見は,まだ実証はなされていないが,両者の分子学的発癌経路が異なることを示唆するものである[Jazaeri et al 2002].このアプローチは最終的には個別の組織病理学的サブタイプの同定につながるものであろう.
遺伝子型と臨床型の関連
がん発症リスクは遺伝子により,また遺伝子内の変異の位置により異なることがある.
BRCA2遺伝子のエクソン11の卵巣がん多発領域(ovarian cancer cluster region;OCCR)に変異が認められる家系では,OCCR以外の部位にBRCA2遺伝子変異が認められる家系と比べて,乳がんよりも卵巣がんの割合が高いと言われている.
BRCA2遺伝子変異陽性患者のいる440家系における1度近親および2度近親に対して卵巣がん,男性乳腺がん,膵がん,前立腺がん,結腸がん,胃がん,メラノーマの有無を調査した[Lubinski et al 2004].ここで得られた所見は以下である:
- 卵巣がん家系では,BRCA2遺伝子の他の部位よりもOCCRに変異を有している頻度が高い.
- ポーランド系家系では他の民族系家系と比べて膵がんの頻度が低かった.このことは,変異の位置と民族的背景の両方がBRCA2遺伝子の生殖細胞系変異を有する家系で観察される表現型の多様さをもたらしていることを示すものである.
浸透度(がん発症リスク)
BRCA1遺伝子およびBRCA2遺伝子の生殖細胞系変異の浸透度は,乳がんと卵巣がんを主要な表現型とする遺伝性乳がん・卵巣がんでもっとも重要な臨床的問題である.浸透度の推定値には,どこから導き出された数値であるかにより,かなりのバラツキが認められる.発症リスクがさまざまであることをもっとも強く示す証拠は,民族集団を限って同一のがん易罹患性の生殖細胞系変異を有する複数の家系に対して行われた調査から得られている(「頻度」の項を参照のこと).蓄積された証拠では,がん易罹患性の生殖細胞系変異を有する患者のなかにがんを発症することなく高齢まで生存する者もいることが示されている.がんを発症する者の間でも,発症年齢や癌種はさまざまである.がん易罹患性の生殖細胞系変異を有する者のなかには50歳以前に複数の原発性がんを発症する者もいるが,同じがん易罹患性の生殖細胞系変異を有する者でもがんの発症が70歳以降であったり[Levy-Lahad et al 2001, Antoniou et al 2008],まったく発症しない者もいるが,なぜそうなるかは明確に説明できない.
「複数乳がん家系」(すなわち,60歳以前に乳がんを発症した罹患者が4人以上いる家系)には,とりわけ卵巣がんも認められる場合には,変異が多く認められ,乳がんと卵巣がん双方のリスクが高いことが示されている.Eastonら[1995]はBRCA1遺伝子変異をヘテロ接合で有する場合,乳がん発症の生涯リスクを80%超としたが,これはこれまで報告された推定値でもっとも高いものである.しかし,このようなリスクはすべての家系におけるリスクを過剰評価している可能性があるため,乳がん発症リスクが40〜60%の範囲である乳がん患者を家族歴を選ばずに対象とした試験が示すように,重症度の低いがんの家族歴を有する家系や「新規診断症例」(incident case)(すなわち,乳がんの家族歴を有するという基準から選択されたのでない乳がん患者)には該当しないことがある[Hopper et al 1999].このような幅広いリスク評価に加えて,BRCA1遺伝子もしくはBRCA2遺伝子に同一の変異を有する家系であっても浸透度にバラツキがあることが示されており,個別の変異を有する人すべてに当てはめることのできる「正確」なリスク評価はないことが窺える.
以下にBRCA1遺伝子もしくはBRCA2遺伝子に変異が同定された患者のがん発症リスクをまとめた.現在,BRCA1遺伝子やBRCA2遺伝子に関連性があることが知られている良性腫瘍や身体異常はない.
BRCA1遺伝子:女性乳がんおよび卵巣がんのリスク
- 家族歴を問わずBRCA1遺伝子変異を有する患者を対象とする[Antoniou et al 2003] 22の地域住民調査研究をまとめて解析したところ[Antoniou et al 2003],70歳までに乳がんを発症する平均リスクは65%(95% CI = 44〜78%),卵巣がんでは39%(95% CI = 18〜54%)であった[Antoniou et al 2003].
- 別の地域住民調査研究では,80歳までにBRCA1関連乳がんを発症するリスクは90%,卵巣がんは24%であった[Risch et al 2006].
- 確認バイアスを修正したところ,BRCA1変異を有する患者に対する10件の研究のメタ解析から,70歳までに乳がんを発症する累積リスクは57%,卵巣がんは40%であると報告された[Chen et al 2006].
- BRCA1遺伝子変異をヘテロ接合で有する場合,乳がんの初回診断から5年以内の対側乳がんを発症するリスクは27%である[Metcalfe et al 2004].
- BRCA1遺伝子関連の乳がんおよび卵巣がんの発症リスクは,両臓器の悪性上皮性腫瘍に限定されるように思われる。
BRCA1遺伝子:その他の関連がんリスク
- 現在,卵管がんはBRCA1遺伝子関連腫瘍群の1つとして広く認められており,その相対リスクは120に上ると報告されている[Medeiros et al 2006].
- また,BRCA1遺伝子変異をヘテロ接合で有する場合,漿液性上皮性卵巣がんと鑑別不能な原発性膜膜漿液性乳頭状腺がんの発症リスクもあり,卵巣摘出術を経た20年後の累積リスクは3.9〜4.3%である[Casey et al 2005, Finch et al 2006].
- BRCA1遺伝子変異をヘテロ接合で有する男性では前立腺がんの発症リスクが増加し,相対リスクは約1.8と推定されるが[Thompson & Easton 2002],BRCA1遺伝子変異の位置によりリスクは大きく異なる[Cybulski et al 2008].さらに,通常このようながんでは診断年齢の若年化は認められない[Giusti et al 2003].
- 一貫性はないが,さまざまな種類のがんがBRCA1関連腫瘍群とみなされている[Brose et al 2002].
- もっとも説得性を持つ関連性は,BRCA1遺伝子変異をヘテロ接合で有する男性における膵がん発症リスク[Lynch et al 2005]および男性乳がん発症リスク[Fentiman et al 2006, Tai et al 2007]の上昇と, 70歳までに乳がんを発症する累積リスク(1.2%)の間に認められる.
- また,Breast Cancer Linkage Consortiumは,(65歳未満のヘテロ接合体女性に限られた数値ではあるが),膵がん(2.3),子宮体がん(2.6),子宮頸がん(3.7)の相対リスクに統計的に有意な増加を報告した[Thompson & Easton 2002].
- 子宮内膜がんとBRCA1/2遺伝子変異との因果関係を示唆するデータには一貫性がない.このような症例はタモキシフェン曝露に関連する可能性がある[Beiner et al 2007].
- 結腸直腸がんリスクが増加したという初回報告は一般に再現されていない.
BRCA2遺伝子:女性乳がんおよび卵巣がんのリスク
- Antoniouら[2003]による22の地域住民調査研究で,70歳までのBRCA2関連リスクは乳がんが45%(95% CI = 33〜54%),卵巣がんが11%(95% CI = 4〜18%)と推定された.
- 別の地域住民調査研究では,80歳までのBRCA2関連の乳がんおよび卵巣がんの発症リスクはそれぞれ41%,8.4%で[Risch et al 2006],これまで報告された卵巣がんの浸透度のなかでもっとも低い数値であった.
- 確認バイアスを修正すると,BRCA2遺伝子変異をヘテロ接合で有する場合,70歳までの累積がん発症リスクは乳がんで49%,卵巣がんで18%と報告された[Chen & Parmigiani 2007].
- 卵巣がんリスクは,BRCA1遺伝子変異をヘテロ接合で有する場合に観察される数値よりも低いが,依然として一般集団(1.4%)よりも高い.BRCA2遺伝子変異をヘテロ接合での卵巣がんの発症は,BRCA1遺伝子のヘテロ接合での卵巣がん発症と比較すると,50歳以後が多い[Risch et al 2001].
- BRCA2遺伝子変異のヘテロ接合の場合,乳がんの初回診断後5年以内の対側乳がん発症リスクは12%である[Metcalfe et al 2004].
- BRCA1遺伝子と同様に,BRCA2関連の乳がんおよび卵巣がんのリスクは両臓器の悪性上皮性腫瘍に限定されているように思われる.
BRCA2遺伝子:その他の関連がんリスク
- 原発性腹膜漿液性乳頭状腺がんと同様に,卵管がんもまたBRCA2遺伝子変異と関連性がある[Aziz et al 2001].卵巣がんと同様,この悪性腫瘍の発症はBRCA1遺伝子変異を有する者と比べて,BRCA2遺伝子変異では少ない[Casey et al 2005].
- 男性乳がんは一般に,BRCA1遺伝子変異よりもBRCA2遺伝子変異との関連が強い.
- BRCA2遺伝子変異を有する男性では,70歳までの乳がん発症累積確率がFentimanら[2006]で6%,Taiら[2007]で6.8%と報告されている.
- BRCA2遺伝子変異を持つ男性における前立腺がんの相対リスクは4.6%である[Breast Cancer Linkage Consortium 1999].BRCA1関連の前立腺がんとは対照的に,発症年齢は通常よりも若年化するようである[Tryggvadottir et al 2007].
- 乳がん家系で膵がんが認められる場合,統計的に有意なBRCA2遺伝子変異の予測因子である可能性があるが[Petersen & Hruban 2003],BRCA1遺伝子変異をヘテロ接合で有する場合にも膵がん発症リスクの上昇が認められている.
- Breast Cancer Linkage Consortiumは,膵がん(3.5),胆嚢胆管がん(5.0),胃がん(2.6),メラノーマ(2.6)における統計的有意な相対リスクの増加を報告した.胆嚢胆管がん,胃がん,メラノーマのBRCA2遺伝子変異との関連性は一貫性がない[Van Asperen et al 2005].
- BRCA1遺伝子と同様,初めに報告された結腸直腸がん発症リスクの上昇との関連性は一般に再現されていない.
個別の集団におけるがんリスク
BRCA1遺伝子に185delAG変異と5382insC変異の2種類のアシュケナージ系創始者変異を有するヘテロ接合の場合,70歳までの乳がん発症リスクは,それぞれ64%(95% CI = 34〜80%)と67%(95% CI = 36〜83%)である[Antoniou et al 2005].同様の数値を卵巣がんで見た場合,14%(95% CI = 2〜24%) )と33%(95% CI = 8〜50%)である.
がん家系の研究から導き出された浸透度の推定値が過剰に上昇することを防ごうと,Satagopanら[2001]は新規に診断された乳がん症例を対象に80歳時点での乳がんの浸透度を調べたところ,BRCA1遺伝子変異のヘテロ接合では59%(95% CI = 40〜93%),BRCA2遺伝子変異のヘテロ接合では38%(95% CI = 20〜68%)であることを見出した.同様の研究デザインを用いてSatagopanら[2002]は70歳時点での卵巣がんの浸透度をBRCA1遺伝子のヘテロ接合では37%(95% CI = 25〜71%),BRCA2遺伝子変異のヘテロ接合では21%(95% CI = 13〜41%)と算出した.
米国では,Chenら[2006]が676のアシュケナージ系家系と非アシュケナージ系民族の1,272家系を対象にして,BRCA1遺伝子のヘテロ接合における70歳までの累積乳がん発症リスクを46%(95% CI = 0.39〜0.54%),卵巣がん発症リスクを39%(95% CI = 0.30〜0.50%)と算出した.
アシュケナージ系のBRCA2遺伝子変異(6174delT変異)のヘテロ接合では,70歳までの乳がん発症リスクは43%(95% CI = 14〜62%),卵巣がん発症リスクは20%(95% CI = 2〜35%)である[Antoniou et al 2005].
アイスランド系のBRCA2遺伝子変異である999del5変異(c.771_775delTCAAA)の乳がん発症率(浸透度)は,50歳までは17%,70歳までは37%であった[Thorlacius et al 1996].
表現促進現象
表現促進現象は観察されていない.
頻度
BRCA1遺伝子およびBRCA2遺伝子の変異によって発症する遺伝性乳がん・卵巣がんは,遺伝性乳がんおよび卵巣がんのどちらにおいてももっとも頻度が高いものであり,すべての民族・人種集団で発症する.BRCA1・2遺伝子変異の全体的な頻度は400〜800人当たり1人 [Ford et al 1994, Claus et al 1996, Whittemore et al 1997]と推定されているが,民族ごとにバラツキがある.
しかし,少数の研究は民族的背景ごとの変異頻度を直接比較している [Szabo & King 1997, Leide & Narod 2002, Olopade et al 2003, Haffty et al 2006, John et al 2007].米国ではアシュケナージ系(中欧系)ユダヤ人に焦点を当てた研究が多い.
以下は,アシュケナージ系ユダヤ人,オランダ人,アイスランド人における特異的なBRCA1遺伝子およびBRCA2遺伝子の生殖細胞系変異を詳説したものであるが,BRCA1遺伝子およびBRCA2遺伝子の創始者変異はその他の幾つかの集団でも同定されている[Ferla et al 2007].
アシュケナージ系ユダヤ人. アシュケナージ系ユダヤ人では,よく研究されている3種類の創始者変異として主に知られるBRCA1・2遺伝子変異が高頻度でみられるために,遺伝性乳がん・卵巣がんの発症リスクが大幅に上昇している.以下のアシュケナージ系ユダヤ人の3種類の変異の頻度を合計すると40人に1人となる[Oddoux et al 1996, Struewing et al 1997, King et al 2003].このように頻度が高いと,アシュケナージ系ユダヤ人に遺伝子検査を勧める際に影響が出てくる(「検査手順」の項を参照のこと).
BRCA1遺伝子
- 187delAG (NC_000017.9)変異. この変異は約1.1%の頻度でアシュケナージ系ユダヤ人に生じる[Struewing et al 1995, Oddoux et al 1996, Roa et al 1996, John et al 2007].
- 5385insC (g.38462606dupC)変異. この変異の頻度は0.1〜0.15%と推定されている[Roa et al 1996].
BRCA2遺伝子
- 6174delT変異 この変異の頻度は約1.5%である[Struewing et al 1995, Oddoux et al 1996, Roa et al 1996, Struewing et al 1997].
診断時65歳未満のアシュケナージ系ユダヤ人女性におけるBRCA1遺伝子変異の頻度は8.3%である[John et al 2007].
BRCA1遺伝子の創始者変異である185delAG変異は,42歳以前に乳がんと診断されたアシュケナージ系ユダヤ人女性の20%に見つかっている[Offit et al 1996].
BRCA2遺伝子の創始者変異である6174delT変異は,42歳以前に乳がんと診断された女性の8%と,それ以外の(unselected)アシュケナージ系ユダヤ人の1.5%に存在する[Berman et al 1996, Roa et al 1996].
オランダ人. これまで言われてきたBRCA1遺伝子変異の大多数はごく少数の塩基に係るものであるが,オランダ人に対する研究でBRCA1遺伝子における3種類の大規模な欠失が同定された.これらの欠失はサザンブロット解析で検出されたものであり,対象となった発症リスクの高いオランダ人家系の1家系では変異の36%を占めていた[Petrij-Bosch et al 1997].オランダ人以外にもBRCA1遺伝子の大規模な欠失が起こりうるが,変異スキャニング,PTT法(protein truncation testing),直接シークエンス法などのより広く用いられているPCR法に基づく変異スクリーニングでは同定されないこともある.
アイスランド人. BRCA2遺伝子変異である999del5変異は,アイスランド人の0.6%と,アイスランド人の乳がん女性の10.4%およびアイスランド人の乳がん男性の38%に認められる[Thorlacius et al 1998].この変異は50歳までに乳がんと診断された女性の17%,50歳以降に乳がんと診断された女性の4%に認められた.999del5変異を有する44人のうち17人(39%)には,1度近親や2度近親にがん患者がいないことから,変異の浸透度が不完全であることが窺われる[Thorlacius et al 1996].
鑑別診断
遺伝性乳がん・卵巣がんに関する遺伝子検査の利用可能性についての最新情報は,GeneTests Laboratory Directoryを参照のこと――編集者注
症候性乳がん.
以下のがん感受性症候群や遺伝子を有する場合,乳がんリスクが高い.多くの場合,遺伝性乳がん・卵巣がんは当該家系で認められる腫瘍の構成からここに掲げられた他の疾患と鑑別可能であるが,なかには分子遺伝学的検査が必要な場合もある.
- リ・フラウメニ症候群は軟部組織腫瘍,乳がん,白血病,骨肉腫,メラノーマ,結腸がん,膵がん,副腎皮質がん,脳腫瘍を伴うがん多発症候群である.リ・フラウメニ症候群の診断は臨床診断基準に基づいてなされる.臨床的にリ・フラウメニ症候群と診断された患者の50%以上で,TP53遺伝子に疾患原因変異が同定される.TP53遺伝子に生殖細胞系変異を有する場合,乳がん発症リスクは44歳までが約49%,生涯リスクが60%である.常染色体優性遺伝疾患である.
- カウデン症候群はPTEN過誤腫諸侯群(PHTS)の1つである.カウデン症候群は甲状腺,乳腺,子宮内膜に良性および悪性の腫瘍を発症するリスクの高い多発性過誤腫症候群である.罹患者は通常,大頭症,外毛根鞘腫,乳頭腫様皮疹を呈し,これらは20歳代後半までに現れる.乳がん発症の生涯リスクは25〜50%で,診断時の平均年齢は38〜46歳である.甲状腺がん(通常,濾胞腺がんで,ときに乳頭がんのこともあるが,髄様がんは生じない)の生涯発症リスクは約10%である.子宮内膜がんの発症リスクはよくわかっていないが,5〜10%に達すると思われる.PTEN過誤腫症候群の診断はPTEN遺伝子変異が同定された場合にのみ下される.常染色体優性遺伝疾患である.
- 遺伝性びまん性胃がん(HDGC)は,びまん性胃がんを常染色体優性遺伝性に発症する疾患である.びまん性胃がんとは,低分化の腺がんが明らかな腫瘍塊を形成せず,胃壁の肥厚(形成性胃壁炎)をきたしながら浸潤していくものである.びまん性胃がんは印環細胞がんあるいは「isolated cell type carcinoma」とも呼ばれる.遺伝性びまん性胃がんの平均発症年齢は38歳である(発症年齢幅は14〜69歳).CDH1遺伝子変異を有する場合,大多数のがんが40歳以前に発症する.80歳までの胃がん発症の累積リスクは,男性で67%,女性で83%である.女性の場合,小葉がん発症リスクも39%ある.
- CHEK2遺伝子 CHEK2遺伝子の1100delC多型(NM_007194.3)は,女性の乳がん発症リスクを約2〜3倍に,男性の乳がん発症リスクを10倍に高めるとみられる[CHEK2 Breast Cancer Case Control Consortium 2004, Bernstein et al 2006, Weischer et al 2007].後期発症乳がん家系と比べて,若年発症乳がん家系との関連性が強いことを示すデータもある.ポーランドにおける大規模な症例対照研究は,CHEK2遺伝子の3種類の創始者変異――c.1100delC変異,c.319+1G>A(IVS2+1G>A)変異,p.Ile157Thr(NM_007194.3)変異――のいずれかを有する場合に甲状腺がん,前立腺がん,結腸がん,腎がんの発症リスクが高まることを明らかにした [Cybulski et al 2004].
- 毛細血管拡張性小脳失調症(A-T)の特徴は,1〜4歳に発症する進行性の小脳性運動失調,眼球運動失調,易感染性,舞踏アテトーゼ,結膜毛細血管拡張,免疫不全,悪性腫瘍の高い発症リスク(とくに白血病やリンパ腫)である.毛細血管拡張性小脳失調症患者は電離放射線に対する感受性が非常に高い.常染色体劣性疾患である.
- 原因遺伝子変異であるATM遺伝子の変異をヘテロ接合で有する場合,がん発症リスクは一般集団の約4倍であり,主に乳がんのリスクが高くなる[Swift et al 1991, Easton 1994, Athma et al 1996, FitzGerald et al 1997, Stankovic et al 1998, Geoffroy-Perez et al 2001, Olsen et al 2001, Teraoka et al 2001, Chenevix-Trench et al 2002, Sommer et al 2002, Bernstein et al 2003, Bretsky et al 2003, Thorstenson et al 2003, Renwick et al 2006].がんの発症リスクは,腫瘍のタイプ,がんの発症年齢,ヘテロ接合の変異がミスセンス変異であるか切断変異であるかなど,他の要因にも影響されると思われる[Gatti et al 2001, Concannon 2002, Scott et al 2002, Spring et al 2002].ATM遺伝子変異を有する女性の約15%が乳がんを発症すると推定されている[Ahmed & Rahman 2006].
- リンチ症候群・遺伝性非ポリポーシス大腸がん(HNPCC) リンチ症候群家系でも乳がんが報告されているが,明らかな関連性は確立していない[Gruber & Petersen 2002, Muller et al 2002].最近Walshら[2010]は,結腸直腸がん家系登録(Colorectal Cancer Family Registry;Colon CFR)の乳がん患者107人のうち35人に,リンチ症候群関連の複数の遺伝子の1つに変異が1つ認められたと報告した.免疫組織化学検査により,35人のうち18人(51%)にミスマッチ修復(MMR)タンパクが存在しないことが示されたが,これは家系内で追跡されたMMR遺伝子変異に対応するものである.典型的なリンチ症候群関連腫瘍が認められない家系において,乳がん組織の解析がMMR欠損の検出に有効な選択肢となりうる可能性があることが結論付けられた.しかし,この試験デザインは限定されたものであったため,Walshら[2010]はリンチ症候群関連変異をヘテロ接合で有する患者で乳がん発症リスクが高まるかについて言及することはできなかった.
- ポイツ-ジェーガース症候群の特徴は,消化管ポリポーシスと粘着色素沈着である.ポイツ-ジェーガース型過誤腫性ポリープは小腸(空腸,回腸,十二指腸の順に多い)に好発するが,多くの患者では胃や大腸にも発生する.Limら[2003]の報告によれば,65歳までの乳がん発症リスクは29%であった.家族歴の有無にかかわらず,かなりの割合で患者にはSTK11遺伝子(LKB1)変異が同定される.常染色体優性疾患である.
- ブルーム症候群の特徴は,重度の成長障害,皮膚および骨格筋異常,免疫機能不全である.乳がん,皮膚がん,気道消化管(頭部,頸部,食道)がん,胃腸のがんを含むさまざまながんが報告されている[Schneider 2002].BLM(RECQL3)遺伝子変異により発症する.常染色体劣性疾患である.
- ワーナー症候群の特徴は,通常,20歳代に加齢に伴う身体所見が現れ,乳がん,肉腫,メラノーマ,甲状腺がん,血液腫瘍などの悪性腫瘍に罹りやすいことである[Schneider 2002].WRN(RECQL2)遺伝子変異により発症する.常染色体劣性疾患である.
- 色素性乾皮症の特徴は,日光過敏,眼球症状であり,皮膚および眼球腫瘍発症リスクは1000倍以上に達する.約30%の罹患者は神経症状を伴う.良性,悪性両方の皮膚腫瘍が高率にみられる.色素性乾皮症では乳腺,脳,子宮,精巣,消化管などの固形腫瘍のリスクも20倍高い[Schneider 2002].色素性乾皮症細胞ではヌクレオチド除去修復(NER)が障害されており,正常細胞と比較して高率に紫外線による細胞死が生じ,DNA合成周期が異常になる.色素性乾皮症の原因遺伝子は,XPA遺伝子,ERCC3(XPB)遺伝子,XPC遺伝子,ERCC2(XPD)遺伝子,DDB2(XPE)遺伝子,ERCC4(XPF)遺伝子,ERCC5(XPG)遺伝子,ERCC1遺伝子,POLH(XP-V)遺伝子である.常染色体劣性疾患である.
臨床医への注:成人発症DRPLAの個別の患者に対する「simultaneous consult」については,![]() を参照のこと.SimulConsult(R)は患者の所見を基に鑑別診断を提供する双方向型診断決定補助ソフトである(登録または施設からのアクセスが必要).
を参照のこと.SimulConsult(R)は患者の所見を基に鑑別診断を提供する双方向型診断決定補助ソフトである(登録または施設からのアクセスが必要).
臨床的マネジメント
初回診断後における評価
BRCA1遺伝子もしくはBRCA2遺伝子にがん易罹患性の生殖細胞系変異を有していると診断された未発症女性に対しては,分子遺伝学的検査の結果開示の際に,今後のスクリーニングや一次病変予防の選択肢についてカウンセリングを行う.
病変の治療
BRCA1遺伝子もしくはBRCA2遺伝子に関連した乳がんや卵巣がんの治療は,非遺伝性の乳がんや卵巣がんの治療と同様である.
一次病変の予防
乳がんをすでに発症した人. BRCA1遺伝子もしくはBRCA2遺伝子の生殖細胞系変異を有する女性で,初発の乳がんに対して温存療法を受けた患者では,同側もしくは対側の乳がん発症リスクがきわめて高いことが幾つかの研究で示されており,一部の専門家は二次がんを予防する目的で両側の予防的乳房切除術を検討している[Sabel 2002].
乳腺腫瘤摘出と放射線照射で乳房温存療法が選択された場合には,予防的卵巣摘出術や綿密な経過観察といったその他の手段が考えられうる[Pierce 2002].
未発症で発症リスクのある人. BRCA1遺伝子もしくはBRCA2遺伝子に生殖細胞系変異を有する人のがん発症リスクを低減させるための方法が幾つか提唱されている.このような予防策には,予防的乳房・卵巣摘出術や化学予防がある.これらはいずれも,高リスク女性に関しては,ランダム化試験で評価されていない.
予防的手術(乳房切除術と卵巣摘出術) 遺伝学的に乳がんや卵巣がんを罹患しやすい人のがん発症リスクを低減する手段として,予防的手術(乳房切除術と卵巣摘出術)が提案されている.発症リスクの高い女性に対するリスク軽減手術の有用性を認める説得力のある報告を行っている研究は数多くあるが,手術の至適時期や術後の長期経過観察のあり方など,幾つかの重要な問題が残っている.
過去30年間でミネソタ州のメイヨー・クリニックで予防的乳房切除術を受けたすべての女性を対象とする後ろ向きコホート試験では,予防的手術により乳がん発症リスクが90%低下したことが示された.メイヨー・クリニックの試験参加女性の3分の1が濃厚な家族歴を有するとみなされた,このような女性でも試験参加者全員と同程度のリスク低下が認められた[Hartmann et al 1999].同一コホートに対するフォローアップ試験では,176人の女性がBRCA1遺伝子やBRCA2遺伝子の生殖細胞系変異を有するかどうかの検査を受けた.BRCA1遺伝子もしくはBRCA2遺伝子変異の生殖細胞系変異を有する26人のうち,追跡期間の中央値である13年間に乳がんを発症した者は皆無であった[Hartmann et al 2001].
より最近の研究では,BRCA1遺伝子もしくはBRCA2遺伝子の生殖細胞系変異を有する483人に対して,乳がん発症頻度が検討された.乳がんと診断されたのは,予防的両側乳房切除術を受けた105人の女性では2人(1.9%),手術を受けなかった対照群378人では184人(48.7%)であり,BRCA1遺伝子もしくはBRCA2遺伝子の生殖細胞系変異を有する女性では予防的両側乳房切除術が乳がん発症リスクを約90%低減させたことが示された[Rebbeck et al 2004].
幾つかの研究では,リスク低減のための卵巣摘出術後の卵巣がんの発症リスクの顕著な(80〜96%)低下が報告されている[Kauff et al 2002, Rebbeck et al 2002, Rutter et al 2003].リスク低減のために切除された組織の組織学的評価から潜在性卵巣がんや原発性卵管腫瘍が幅広く見つかっており,この所見は手術時に卵巣と卵管をともに摘出することがよいということを示している[Leeper et al 2002, Olivier et al 2004, Powell et al 2005].しかし,リスク軽減のための卵巣摘出術を行っても原発性腹膜腫瘍のリスクは残っており,手術後の発症率は約2%である[Piver et al 1993, Casey et al 2005].
また,Rebbeckら[2004]は予防的両側卵巣摘出術を受けた女性の乳がん発症リスクが53%低下したと報告した.これらの報告はOlopadeとArtioliによる報告[2004]と合致している. 1,079人の女性を30〜35カ月(追跡期間中央値)を追跡した多施設共同試験では,予防的卵巣摘出術を受けたヘテロ接合の全員に乳がん発症リスクの低下が認められたが,BRCA1遺伝子変異のヘテロ接合女性と比べてBRCA2遺伝子変異のヘテロ接合女性に大幅な発症リスクの低減が認められたことが示された [Kauff et al 2008].予防的手術を行う至適時期や長期経過観察のあり方など,予防的手術に関する重要な問題点は幾つか残っている.手術によってもたらされる閉経による副作用(血管運動性症状,膣乾燥,骨粗鬆症,心疾患の発症リスクの上昇など)も考慮されなければならない.
化学予防. Gailモデルから乳がん発症リスクが高いと判定された女性に対するタモキシフェン(部分的エストロゲン拮抗薬)治療に関するランダム化臨床試験では,治療群で乳がん発症リスクが49%低下したと報告された[Fisher et al 1998].Gailら[1999]は,乳がん発症リスクが高い50歳未満の女性に対する予防的なタモキシフェン投与がきわめて有効であると結論付けた.しかし,タモキシフェンはエストロゲン受容体陽性乳がんの発症率を低下させるが,エストロゲン受容体陰性乳がんの発症率は低下させなかった.BRCA1遺伝子の生殖細胞系変異を有する女性に発症する乳がんはエストロゲン受容体陰性であることが多いため(「自然経過」の項を参照),タモキシフェン投与がより有効であるのはBRCA2遺伝子の生殖細胞系変異を有する女性であろうことが予測される.このため,BRCA1遺伝子やBRCA2遺伝子の生殖細胞系変異を有する女性に対する予防的タモキシフェン投与の有効性を調べる幾つかの臨床試験が実施されている.
ランダム化試験のサブセット解析で,BRCA1遺伝子やBRCA2遺伝子の変異を遺伝的に受け継いでいるががんを発症していない女性に関して,乳がんの発症頻度に対するタモキシフェンの効果が評価され,タモキシフェンによりBRCA2遺伝子の生殖細胞系変異を有する健康女性の乳がん発症リスクが62%低下することが示された[King et al 2001].BRCA1遺伝子やBRCA2遺伝子の生殖細胞系変異を有する538人の女性に対する症例対照研究では,タモキシフェン投与が対側乳がん発症リスクの50%低下に関連していた[Narod et al 2000].最近行われた491人の遺伝性乳がん患者女性に対する後ろ向きコホート研究では,10年間で対側乳がん発症リスクが41%低下したことが示された[Metcalfe et al 2005a].タモキシフェンはBRCA1遺伝子やBRCA2遺伝子の生殖細胞系変異を有する女性の乳がん発症リスクを低下させる効果があるように思われるが,他のリスク低減法と比べるとタモキシフェン投与の効果は限られたものである[Metcalfe et al 2005b].
タモキシフェン治療の重大な有害事象には,投与を受けた者では投与を受けていない者と比べて,子宮内膜がんや血栓塞栓症(肺塞栓症など)が高頻度に発症することが挙げられる.
授乳. 最近行われた研究では,BRCA1遺伝子の生殖細胞系変異を有する女性で累積の総授乳期間が1年以上である場合,乳がんの発症リスクが統計的有意に低下したことが示された[Jernstrom et al 2004].
経過観察
BRCA1遺伝子やBRCA2遺伝子に生殖細胞系変異を有する人のがん発症リスクを低下させる方法が幾つか提案されている.そのなかにがんのスクリーニング検査も含まれる.がんスクリーニング検査に関しては,高リスク女性に対するランダム化試験や症例対照研究による評価は行われていない.
乳がんスクリーニング. 米国総合がんセンターネットワーク(NCCN)は遺伝性乳がんや卵巣がんのリスクを有する人への対応に関する実施指針を発表した[Daly et al 2010].![]() 参照のこと(要登録).
参照のこと(要登録).
以下にこの指針で推奨される乳がんスクリーニングを掲げる:
- 成人期の早いうちから毎年の乳房の自己チェック
- 25歳以降は半年ごとの病院での乳房触診
- 25〜35歳以降は毎年のマンモグラフィーおよび乳MRI検査
家系内でもっとも早い発症年齢に基づいて各個人に応じたスクリーニングを行うこと.
最近の研究では,BRCA1遺伝子やBRCA2遺伝子の生殖細胞系変異を有する女性に対する乳MRIスクリーニングの有効性が評価されている[Kriege et al 2004, Warner et al 2004, Warner & Causer 2005].このような研究のうちの1つでは,BRCA1遺伝子やBRCA2遺伝子の生殖細胞系変異を有する女性に対する4種類の乳がんスクリーニング検査方法(マンモグラフィー,超音波検査,MRI,乳房触診検査)について,感度と特異性が比較された(表3).BRCA1遺伝子やBRCA2遺伝子の生殖細胞系変異を有する236人のカナダ人女性がこれら4種類の方法について評価されたが,そこから22のがんが発見された.著者らはBRCA1遺伝子やBRCA2遺伝子の生殖細胞系変異を有する女性の乳がんスクリーニング検査はMRIに基づくスクリーニング検査が標準となるだろうと結論づけた[Warner et al 2004].最近米国総合がんセンターネットワーク(NCCN)は,BRCA1遺伝子やBRCA2遺伝子の生殖細胞系変異を有する女性に対しては標準的なマンモグラフィーに加えて乳MRI検査を推奨する発表を行った[Daly et al 2010].
表3. BRCA1遺伝子やBRCA2遺伝子関連乳がん女性のスクリーニング検査:4種類の方法の感度と特異性
癌発見のためのスクリーニング方法 |
がん検出数(総数=22) |
感度 1 |
特異性 |
MRI |
17 |
77% |
95.4% |
マンモグラフィー |
8 |
36% |
99.8% |
超音波検査 |
7 |
33% |
96% |
乳房触診検査 |
2 |
9.1% |
99.3% |
1. 4種類の検査感度の合計は95%である.
マンモグラフィーと乳房触診検査の感度の合計は45%である.
BRCA1遺伝子やBRCA2電子の生殖細胞系変異を有する男性も乳がん発症リスクが高い.正式に認められた経過観察スケジュールはないが,乳房の自己チェックのトレーニングを行って毎月定期的に自己チェックを行うことが推奨されている.加えて,半年ごとの乳房触診検査や,初回のマンモグラフィー検査で女性化乳房や乳腺密度の上昇が検出された場合には,継続的に毎年マンモグラフィー検査を行って経過観察を行うことも推奨されている[Daly et al 2003].
卵巣がんスクリーニング. 利用可能な卵巣がんスクリーニング方法(経膣超音波検査,血清CA-125濃度測定)には感度,特異性とも限界があり,卵巣がんによる死亡率の低下はみられていない[Clarke-Pearson 2009].しかし,予防的卵巣摘出術を選択しない女性では,35歳以降,もしくは家系でもっとも早い発症年齢に基づいて,半年ごとに経膣超音波検査とCA-125濃度測定を開始することを考慮してもよい.
前立腺がんスクリーニング. BRCA1遺伝子やBRCA2遺伝子の生殖細胞系変異を有する男性では,前立腺がん発症リスクが高いとみられるため,前立腺がんスクリーニングに関する選択肢について情報提供すべきである[Burke et al 1997].米国がん協会は一般集団に対して,50歳以降,直腸診とPSA(前立腺特異抗原)検査を毎年行うことを推奨しているが,「家系的にきわめて罹りやすい」者を含む高リスク群に対してはより早期のスクリーニングを考慮するよう勧めている[Mettlin et al 1993].したがって,BRCA1遺伝子やBRCA2遺伝子の生殖細胞系変異を有する男性に対しては,40歳から前立腺がんの検査を受けることが一貫して推奨されている.
膵がんスクリーニング. 膵がんはBRCA2遺伝子関連腫瘍であるという認識が確立している.しかし,膵がんの易罹患性とBRCA1遺伝子変異の生殖細胞系変異との関連性はそれほど強くない.一般に,膵がんの症状がない人に対するスクリーニングは推奨されていないが,臨床研究レベルでは可能である.
メラノーマ. 皮膚および眼球のメラノーマはどちらもBRCA2遺伝子関連腫瘍である.1年に1回の専門医による皮膚科および眼科での診察が推奨される.
リスクのある親族の検査
家系内にがんを罹患しやすいBRCA1遺伝子やBRCA2遺伝子の生殖細胞系変異が同定されたならば,リスクのある親族の検査により家系内変異を持つ血縁者が同定できるため,定期検査や,がんが発見されたときに早期介入が必要となる人を特定することができる.
遺伝カウンセリングとして扱われるリスクのある親族への検査に関する問題は「遺伝カウンセリング」の項を参照のこと.
研究中の治療法
BRCA1遺伝子やBRCA2遺伝子のシグナル経路を標的とした治療法の研究が進められている[Farmer et al 2005].これらの詳細についての記述は,GeneReviewが目的とするところではない.
種々の疾患に対する臨床試験についてはClinicalTrials.govを参照のこと.
その他
ホルモン補充療法. 一般集団に対する研究で,閉経後女性の長期的なエストロゲン補充療法が乳がん発症リスクを高める可能性が示されたが,更年期症状に対する短期的な使用に関しては認められていない.しかし,ホルモン補充療法に関するランダム化プラセボ対照試験で,比較的短期間のエストロゲンと黄体ホルモンの服用でも乳がんの発症頻度が高まることが示された[Chlebowski et al 2003].
Rebbeckら[2005]は,BRCA1遺伝子やBRCA2遺伝子の生殖細胞系変異を有する462人の女性コホートについて,予防的両側卵巣摘出術後のホルモン補充療法に関連した乳がん発症リスクを評価したところ,予防的両側卵巣摘出術後はいかなるホルモン補充療法によっても,手術によってもたらされた乳がん発症リスクの低下に統計的に有意な変化は認められなかったと報告した.手術後の追跡期間は3.6年であった.BRCA1遺伝子やBRCA2遺伝子の生殖細胞系変異を有する女性における続発性乳がん発症リスクについて,短期的なホルモン補充療法は予防的両側卵巣摘出術の予防的効果を損なわないと結論付けられた.この試験に対応する症例対照研究ではBRCA1遺伝子変異を有する472人の閉経後女性が対象とされたが,ホルモン補充療法と乳がん発症リスクの低下に関連性があるとされた(オッズ比= 0.58;95%信頼区間=0.36〜0.96) [Eisen et al 2008].
経口避妊薬. ある症例対照研究では,3年以上経口避妊薬を服用しているBRCA1遺伝子やBRCA2遺伝子の生殖細胞系変異を有する女性で卵巣がん発症リスクが低下することが示された[Narod et al 1995].これらのデータは,経口避妊薬の服用により卵巣がん発症リスクが低下することを示した一般集団を対象とする研究データに合致するものである.この症例対照研究では,経口避妊薬の乳がん発症リスクへの影響などのその他の影響は評価されていない.
より最近行われた研究では,経口避妊薬の服用に関連した卵巣がん発症リスクの低下が示されており,服用期間が長くなればなるほど発症リスクが低下することが示された.Whittemoreら[2004]はBRCA1遺伝子やBRCA2遺伝子の生殖細胞系変異を有する451人の女性における経口避妊薬の服用状況を調べて,経口避妊薬をこれまで使用したことのある女性(”ever-users”)では14%,長期間服用者では38%,卵巣がん発症リスクが低下したことを見出した.これは,(一般集団と比較すると幾分関連性は弱いが)一般集団で認められた発症リスク低下と合致するものである[Whittemore et al 2004].さらに,現在(1975年以降)使われている経口避妊薬がBRCA1遺伝子やBRCA2遺伝子の生殖細胞系変異を有する女性の若年発症の乳がん発症リスクを高めると言われていないため,BRCA1遺伝子やBRCA2遺伝子の生殖細胞系変異を有する女性への経口避妊薬の適用を禁忌とすべきでないことが裏付けられる[Milne et al 2005].
喫煙はBRCA1遺伝子やBRCA2遺伝子の生殖細胞系変異を有する人の乳がん発症リスクを高める危険因子ではないようである[Ghadirian et al 2004].
遺伝クリニックは,患者や家族に自然経過,治療,遺伝形式,患者家族の遺伝的発症リスクに関する情報を提供とするとともに,患者サイドに立った情報も提供する.Gene Test Clinic Directoryを参照のこと.
患者情報 本疾患の支援グループや複数疾患にまたがった支援グループについては「患者情報」を参照のこと.これらの機関は患者やその家族に情報,支援,他の患者との交流の場を提供するために設立された.遺伝カウンセリング
「遺伝カウンセリングは個人や家族に対して遺伝性疾患の本質,遺伝,健康上の影響などの情報を提供し,彼らが医療上あるいは個人的な決断を下すのを援助するプロセスである.以下の項目では遺伝的なリスク評価や家族の遺伝学的状況を明らかにするための家族歴の評価,遺伝子検査について論じる.この項は個々の当事者が直面しうる個人的あるいは文化的な問題に言及しようと意図するものではないし,遺伝専門家へのコンサルトの代用となるものでもない.」
遺伝形式
BRCA1遺伝子およびBRCA2遺伝子の生殖細胞系変異は常染色体優性で遺伝する.
血縁者のリスク
BRCA1遺伝子やBRCA2遺伝子の変異を有する発端者の両親
- BRCA1遺伝子やBRCA2遺伝子に生殖細胞系変異を有する人はほとんど全員が,親の1人から変異を受け継いでいる.
- 変異の浸透度,変異を有する親の性別,変異を有する親の年齢,その他の要因により,親にがんの診断が下っている場合もあれば,下っていない場合もある.
- どちらの家系にリスクがあるかを確定するために,BRCA1遺伝子やBRCA2遺伝子の生殖細胞系変異を有する人の両親に対して,分子遺伝学的検査を勧めるとよい.
- どちらの親にもBRCA1遺伝子やBRCA2遺伝子に生殖細胞系変異が同定されない場合がある.新生突然変異によってBRCA1遺伝子もしくはBRCA2遺伝子の生殖細胞系変異を有する人の数は不明であるが,少数と考えられる[Tesoriero et al 1999, Robson et al 2002, van der Luijt et al 2001].
- 発端者の同胞のリスクは発端者の両親の遺伝学的状況によって決まる.
- 親の片方にBRCA1遺伝子もしくはBRCA2遺伝子に生殖細胞系変異が認められるならば,孤発例の同胞がBRCA1遺伝子やBRCA2遺伝子の生殖細胞系変異を受け継いでいるリスクは50%である.
- しかし,がん発症リスクは変異の浸透度や性別や年齢といった多数の要因によって決まる.
- BRCA1遺伝子やBRCA2遺伝子の生殖細胞系変異が同定された人の子が同じ変異を受け継ぐ確率は50%である.
- しかし,がん発症リスクは変異の浸透度や性別や年齢といった多数の要因によって決まる.
BRCA1遺伝子やBRCA2遺伝子の変異を有する発端者のその他の血縁者
その他の血縁者のリスクは発端者の両親の遺伝学的状況により決まる.BRCA1遺伝子やBRCA2遺伝子の生殖細胞系変異を有する親の家系にはリスクがある.正確な発症リスクは家系内での位置により決まる.
遺伝カウンセリングに関連した問題
見かけ上新生突然変異を持つ家系への配慮. 常染色体優性疾患の発端者の両親のどちらにも疾患原因の生殖細胞系変異が認められず,疾患の臨床症状がない場合,発端者が新生突然変異を有している可能性がある.しかし,父親や母親が異なる場合(生殖補助医療など)や,公開されていない養子縁組といった医学的でない原因も検討する必要がある.稀ではあるが,BRCA1遺伝子やBRCA2遺伝子でも新生突然変異が報告されている.
家族計画
- 遺伝リスクの決定や出生前診断の利用について話し合う最適な時期は妊娠前である.
- 罹患している若年成人や発症リスクのある若年成人に対して遺伝カウンセリング(子への潜在的リスクや生殖手段)を提供することは妥当である.
遺伝的がん発症リスクの評価と遺伝カウンセリング. 分子遺伝学的検査を用いるか用いないかにかかわらず,がん発症リスク評価によってリスク保持者を同定することに対する医学的,心理的,倫理的問題を総合的に扱ったものには,「遺伝的ながん発症リスク評価と遺伝カウンセリングに関する要点」(米国国立癌研究所作成のPDQ(R)の一部)がある.
リスクのある無症状の成人血縁者. 一般に,BRCA1遺伝子やBRCA2遺伝子の生殖細胞系変異を有する者の血縁者は,同一の変異を有しているリスク,分子遺伝学的検査に関する選択肢,がん発症リスク,推奨されるがんスクリーニング検査や予防的手術に関して,カウンセリングを受けるべきである.
分子遺伝学的検査についてより詳しく知りたいと考える人に対しては,以下の議論を含めた検査前の教育を実施することが勧められる[American Society of Clinical Oncology 1997, Geller et al 1997, McKinnon et al 1997, American Society of Clinical Oncology 2003]:
- 分子遺伝学的検査を受けたいと思う動機と検査への先入観(発症リスクのある無症状の成人親族のなかには,生殖,経済的問題,職業選択といった個人的決定を行うために検査を希望することがあれば,ただ単に「知る必要がある」という理由で検査を希望する場合もある.)
- (検査を希望する)個人の,がん発症リスクについての認識
- (検査を希望する)個人が,検査を受ける心構えができているかどうか,および検査実施の至適時期
- DNAバンクなどの遺伝子検査以外の方法
- 遺伝子検査ではがんを発症しているかはわからないこと
- (検査を希望する)個人に対するサポート態勢と,さらなる心理的サポートの必要性
- (検査を希望する)個人のプライバシー保護と自発性の必要性
- 検査が陽性,陰性,もしくは判断不能であった場合の以下の要因に対する影響:
- がん発症リスク
- がんスクリーニング検査のスケジュール
- 他の血縁者のリスク
- 保険加入や就職(遺伝情報差別禁止法が可決されたように,連邦法規や州法が健康保険加入や就職に際しての差別に反対しているとはいっても,遺伝的にがんに罹患しやすいことが判明した人は健康保険の加入時や就職で差別を受けるおそれがある.)
- 心理的状況(うつ,不安,罪悪感など)
- 配偶者,子,親族,友人との関係
発端者で同定されたがん易罹患性生殖細胞系変異は受け継いでいないが発症リスクを有する成人親族のがん発症リスクは,個人的な危険因子により,一般集団と同程度もしくはそれを上回ると考えられる.たとえば,家系特異的BRCA1遺伝子やBRCA2遺伝子の変異はないが発症リスクのある血縁者女性は,乳生検で非定型の乳管過形成が見つかった場合などでは依然として乳がん発症リスクが高い.
がん発症リスクが一般集団と同等であることが確定した血縁者は,米国がん協会や米国総合がんセンターネットワーク(NCCN)が平均的なリスクを有する人に推奨している適切ながんスクリーニング検査を受けることが望ましい.注:このような推定は,家系内罹患者がBRCA1遺伝子もしくはBRCA2遺伝子の分子遺伝学的検査を受けていなかったり,家系内罹患者にBRCA1遺伝子やBRCA2遺伝子に変異が同定されなかったためにBRCA1遺伝子やBRCA2遺伝子の生殖細胞系変異が同定される可能性のない人には該当しない.
小児期のリスクのある無症状者の検査. 成人発症の病態(BRCA1遺伝子やBRCA2遺伝子の生殖細胞系変異を含む)のリスクがある18歳未満の無症状者の検査実施には,未成年のインフォームドコンセントの問題,その年齢では確立された経過観察や予防法がないこと,烙印付けや差別の問題などを含めた法的な懸念が存在する.このような状態での検査は,通常勧められない.(子どもに対する遺伝学的検査に関する米国遺伝カウンセラー学会の決議文も参照のこと.米国人類遺伝学会と米国臨床遺伝学会は考慮すべき点として,小児思春期の遺伝学的検査の倫理的,法的,心理的影響を挙げている.)
DNAバンクは,将来の使用のために,通常は白血球から調整したDNAを貯蔵しておくことである.検査手法や,遺伝子,変異,疾患への理解は将来改善する可能性があり,患者のDNAを貯蔵しておくことは考慮されるべきである.ことに現在行っている分子遺伝学的検査の感度が100%ではないような疾患に関してはDNAの保存は考慮すべきかもしれない.このサービスを行っている機関についてはDNA bankingの項を参照のこと.
出生前診断
BRCA1遺伝子やBRCA2遺伝子の生殖細胞系変異に対する出生前診断は技術的には,通常胎生週数15〜18週頃に実施される羊水検査や胎生週数10〜12週頃に実施される絨毛生検(CVS)により採取された胎児細胞のDNA分析により技術的には可能である.出生前診断の実施以前に,家系内患者の疾患原因アレルが同定されていることが条件である.
注:胎生週期とは最終月経の第1日から換算するか,超音波による計測によって算出される. 可能である.
知能に影響を与えることがなく,また何らかの治療が可能であるBRCA1遺伝子やBRCA2遺伝子関連の遺伝性乳がん/卵巣癌のような成人発症のがんに罹りやすくなる生殖細胞系変異に対して出生前診断を希望することは一般的でない.出生前診断の実施は,専門医のあいだでも家族によっても考え方が異なるだろう.特に,検査が妊娠中絶を考慮したうえで行われる場合にはなおのことである.たいていの医療機関は出生前診断を受けるかどうかの決定は両親の選択に委ねるだろうが,この問題に関しては慎重な議論が必要である.
着床前診断(PGD) は事前にBRCA1遺伝子やBRCA2遺伝子の生殖細胞系変異が同定されている家系では実施可能である.着床前診断を行っている施設に関しては![]() を参照のこと.
を参照のこと.
注:GeneTests Laboratory Directoryの掲載施設で実施可能な臨床検査を載せることがGeneReviewsの方針である.ここで掲載されている検査は必ずしも著者や編集者や審査者の推奨を反映するものではない.
更新履歴
- Gene Review著者: Nancie Petrucelli, MS, Mary B Daly, MD, PhD, Julie O Bars Culver, MS, Gerald L Feldman, MD, PhD, FACMG.
日本語訳者: 櫻井晃洋(信州大学医学部遺伝医学・予防医学講座) )
Gene Review 最終更新日: 2007.7.19. 日本語訳最終更新日: 2008.3.24. - Gene Review著者: Nancie Petrucelli, MS, Mary B Daly, MD, PhD, Gerald L Feldman, MD, PhD, FACMG.
日本語訳者: 窪田美穂(ボランティア翻訳者),櫻井晃洋(信州大学医学部附属病院遺伝子診療部)
Gene Review 最終更新日: 2011.1.20. 日本語訳最終更新日: 2011.3.20.