セリアック病
(Celiac Disease)
[同義語: Ceœliac Disease, Celiac Sprue, Nontropical Sprue, Gluten-Sensitive Enteropathy]Gene Reviews著者: K Taylor, MS, PhD, CGC, Benjamin Lebwohl, MD, MS, Cara L Snyder, MS, CGC, and Peter HR Green, MD.
日本語訳者: 和田宏来 (県西総合病院小児科/筑波大学大学院小児科)
Gene Reviews 最終更新日: 2015.9.17. 日本語訳最終更新日: 2017.12.8.
要約
疾患の特徴
セリアック病は全身性の自己免疫疾患であり、消化器症状(下痢・体重減少・腹痛・食欲不振・乳糖不耐、腹部膨満・易刺激性)や極めて多様な非消化器症状(鉄欠乏性貧血・疱疹状皮膚炎・慢性疲労・関節痛/炎症・片頭痛・抑うつ・注意欠陥性障害・てんかん・骨粗鬆症/骨減少症・不妊/習慣流産・ビタミン欠乏・低身長・成長障害・思春期遅発症・エナメル質異常・自己免疫疾患)を合併しうる。軽度~重度の消化器症状を特徴とする古典的なセリアック病は、消化器症状を欠く非古典的なセリアック病よりも多くはない。
診断・検査
セリアック病の診断は、小腸生検による特徴的な組織学的所見やグルテン除去食による臨床的/組織学的な改善によって行われる。ほとんどのセリアック病患者はセリアック病関連抗体を有する。セリアック病の発症には、HLAクラスⅡ遺伝子HLA-DQA1やHLA-DQB1の特異的なアレル変異が存在しないといけない。一般人口の30%は1つ以上のセリアック病関連アレルを有しているが、セリアック病を発症するのはわずか3%であるため、セリアック病関連HLAアレルの有無は診断の決め手とはならない。しかし、同アレルを認めない場合は基本的に除外される。
臨床的マネジメント
症候の治療:
生涯にわたり厳格なグルテン除去食(小麦・ライ麦・大麦を避ける)を順守する。栄養障害(鉄・亜鉛・カルシウム・脂溶性ビタミン・葉酸)の治療を行う。骨粗鬆症に対する標準的な治療を施行する。
一次病変の予防:
生涯にわたってグルテン除去食を続ける。
定期検査:
グルテン除去食が有効な有症状患者に対しては、定期的な身体診察や成長・栄養状態・非消化器症状の評価を行う。診断後は1~3年おきに小腸生検を繰り返す。グルテン除去食が有効ではない有症状患者に対しては、定期的に難治性セリアック病、潰瘍性腸炎(ulcerative enteritis)、T細胞性リンパ腫、その他の消化器がんの評価を行う。
避けるべき薬物/環境:
食物中のグルテン
リスクのある親族への検査:
発端者の(幼少児を含む)第一度近親者に対する分子遺伝学的検査を行い、既知のセリアック病感受性アレルを有する者に対しては、疾患早期からグルテン除去食を開始できるようにセリアック病の早期徴候がないか経過観察する。
遺伝カウンセリング
セリアック病は多因子疾患であり、同疾患の疾患感受性と関連することが知られているHLA-DQA1およびHLA-DQB1アレル変異、それよりは知られていない非HLA遺伝子変異、グリアジン(グルテンの亜成分)、およびその他の環境因子の相互作用によって起こる。親族のリスク評価に関していくらか経験的なデータはある。
診断
セリアック病の診断は、グルテンを含む食事を継続しながら上部消化管内視鏡を行い、十二指腸生検で特徴的な組織学的変化(表1)を認める場合に確定する。
十二指腸生検の適応は以下である。
- 血清学的にセリアック病が示唆されるとき。最も多いのは組織トランスグルタミナーゼ(TTG)に対するIgA抗体の上昇である(「検査戦略」「グルテン除去食を行っている有症状患者」「特異的セリアック病関連抗体検査」を参照)。
- 適応に限らず内視鏡検査時にルーチンに行う。
- 血清学的検査(感度は不十分)で陰性でもセリアック病の可能性が高いと思われるとき。
他の診断アプローチとして以下が提唱されている。
- 欧州小児栄養消化器肝臓学会によるガイドラインでは以下のような条件がそろえば十二指腸生検は施行しなくても診断できるとしている。TTG IgAが高値(正常上限の10倍を超える)の有症状患者で、2回目の採血で筋内膜抗体の上昇を認め、セリアック病に関連するHLAハプロタイプ(DQ2もしくはDQ8)を認める場合。新しいガイドラインでは、このような疾患の可能性が高い状況下では、両親は子どもの上部消化管内視鏡検査を希望しないかもしれない現実を受け入れている。
注:このガイドラインは一部議論の余地を残しており、米国では生検を行わずにセリアック病を診断することを推奨したガイドラインは現在のところ存在しない。
- 以下の5つの特徴のうち、4つ認めた場合にセリアック病と診断できるとする"4/5ルール"(Catassi & Fasanoら[2010]によって提唱されSaponeら[2012]によって記述された)が存在する。
- セリアック病の典型的な症候を認める。
- 高力価のセリアック病抗体を認める。
- 関連するHLAハプロタイプ(DQ2もしくはDQ8)を認める。
- 小腸生検で腸疾患(enteropathy)を認める。
- グルテン除去食が有効である。
"4/5ルール"は公的なガイドラインでは認められておらず、現在のところ診断のためには全例で十二指腸生検を施行することが標準的である。ただし、欧州ガイドラインで示された有症状患者が例外となる可能性はある。
セリアック病の診断に関する総論は他にもHill & Rakitt [2014]やGuandalini & Assiri [2014]によって記述されている。診断・治療に関する主な推奨はOxentenko & Murray [2015]によってまとめられている。
セリアック病の診断を確定する検査戦略
専門施設における臨床経験や文献のレビューに基づき、以下の検査戦略が推奨される。
グルテン除去食を開始する前は有症状であった患者
注:症候については「臨床的特徴」の項を参照。
特異的セリアック病関連抗体検査 Leffler & Schuppan [2010]によってセリアック病関連抗体検査についてのレビューが記述されている。もっとも有用な単一抗体検査は組織トランスグルタミナーゼ(tTG)IgAである。セリアック病の血清学的検査の感度や特異度は2つ以上の抗体検査を用いることにより向上する。IgA欠損症を除外するために、セリアック病関連抗体検査と同時に総IgA値も測定することが重要である。
- 組織トランスグルタミナーゼ(tTG)IgA 感度・特異度が高くコストは比較的低いこと、煩雑さがないことや信頼性の面などから、初回検査として血清組織トランスグルタミナーゼ(tTG)免疫グロブリンA(IgA)の測定がしばしば推奨される。セリアック病の自己免疫プロセスにより、この腸管蛋白に対する抗体が産生される。
- 抗脱アミド化グリアジン関連ペプチド(a-DGP)IgA・IgG抗体 この検査は合成脱アミド化グリアジン関連ペプチド(DGPs)に結合する抗体を検出する。セリアック病の発症率の高い集団を検査した予備的研究において、活動期のセリアック病に対する両方の抗体アイソタイプ(IgAおよびIgG)の感度および特異度は高いことが示されている。幼少児においてDGP抗体価は血清tTG-IGAより先に上昇している可能性がある。しかし、全ての抗体検査がそうであるように、少数の患者では偽陰性を示すことがある。
- 筋内膜抗体(EMA)IgA 血清EMA IgA濃度の特異度は最も高いが(~99%)、血清tTG IgAよりも費用が高く、測定に時間を要し、偽陰性になりやすい可能性がある。間接免疫蛍光抗体法であるため、血清EMA IgA濃度は測定者によって左右され、それが感度に影響を与える。経験の豊富な施設で測定された場合、tTG抗体検査よりも特異度は高く(100%に近い)、肝硬変患者で有用である。
- 選択的IgA欠損症を評価するための血清総IgA濃度測定 選択的IgA欠損症の原因は不明であるが、一般集団の発生率は700人に1人である。原因は不明だが選択的IgA欠損症の発生率は一般集団よりもセリアック病患者のほうが高い(50人に1人)。
選択的IgA欠損症患者ではIgAが産生されないため、セリアック病関連IgA抗体であるtTG IgAやEMA IgAは認められない。そのため、同疾患患者においては代わりにセリアック病関連IgG抗体(tTG IGもしくはDGP-IgG)を測定するべきである。
特異度が比較的低いため、第一世代グリアジン抗体(AGA)測定はもはや推奨されないことに注意されたい。選択的IgA欠損症の症例においてはtTG IgGおよびDGP IgGを測定するべきである。陽性の場合、もしくははっきりしない場合は次に小腸生検を施行するべきである。
臨床的にセリアック病の疑いが強い場合、もしくは明らかな吸収不良を認める場合、特異的セリアック病関連抗体検査の結果に関係なく小腸生検を施行するべきである。
小腸生検 セリアック病診断のゴールドスタンダードである特徴的な組織学的所見には、部分的/完全な絨毛萎縮、陰窩過形成、上皮内リンパ球(IELs)の増加などがある。腸管病変の動的な進展や軽症セリアック病の頻度に基づいて、Marsh[1992]は診断を確定するためおよびグルテン除去への反応を評価するための4段階のグレード分類を提唱した(表1)。
これらの変化はセリアック病に特有のものではないが、グルテン除去後の腸管損傷の回復はセリアック病に特有である。
生検における陽性予測度は、その集団における他の原因による腸症と比較したセリアック病の相対的な発生率によって決まる。
表1 セリアック病の腸管病変の分類
| タイプ | 粘膜所見 |
|---|---|
| ステージ0 前浸潤性病変 | 正常 |
| ステージ1 浸潤性病変1 | 上皮内リンパ球の増加 |
| ステージ2 過形成病変 | ステージ1の変化+過形成陰窩 |
| ステージ3 破壊性病変2 | ステージ2の変化+ ・部分絨毛萎縮(3a) ・亜全絨毛萎縮(3b) ・全絨毛萎縮(3c) |
| ステージ4 低形成病変3 | 陰窩低形成を伴う全絨毛萎縮 |
Hillら[2005]
- ステージ1は、炎症性腸疾患(IBD)、非ステロイド性抗炎症薬(NSAIDs)の使用、シェーグレン症候群、ヘリコバクター・ピロリ感染胃炎、そしておそらく食物不耐症といった他疾患のプロセスでも見られうる。
- ステージ3はセリアック病の古典的な病変で最もよくみられる組織所見であるが、熱帯性スプルー、小腸内細菌異常増殖(SIBO)、NSAIDsの使用、急性胃腸炎、自然に軽快する胃腸炎など他の病態でも認めうる。
- ステージ4はときに高齢者でみとめられる。
以下のような状況下では、小腸生検はセリアック病の組織変化を検出できないことがある。
- グルテン除去食
- 疾患の早期
- まばらな粘膜病変
- 消化性疾患(peptic changes)によってセリアック病の所見がはっきりしない場合
- 生検標本の数が不十分な場合
- 鏡検でスライドの誤認がある場合
- 潜在性セリアック病(スクリーニングのセリアック病関連抗体検査は陽性だが小腸生検で絨毛萎縮を認めない場合と定義される)
偽陽性も不十分な生検(poorly oriented biopsies)を過大に評価することによって起こる。
ガイドラインは、セリアック病の組織学的特徴がまばらにしか見られないことを鑑み、評価のためには4~6個の十二指腸生検標本を採取することを推奨している。米国ではガイドラインはあまり遵守されていないが、推奨された数の生検標本を提出する努力が必要である。
- セリアック病関連抗体検査を認めないがなおも疾患が疑われる場合、セリアック病関連HLAアレルの分子遺伝学的検査は疾患の除外もしくは感受性をみるのに有用な可能性がある(「グルテン除去食を行っている有症状患者」「分子遺伝学的検査」を参照)。
- セリアック病の診断は、小腸生検で特徴的な組織学的変化を認めグルテン除去食で臨床的/組織学的に改善がみられたときに確定する。しかし、例外的に自然軽快する腸炎(self-limited enteritis)や熱帯性スプルーの患者はグルテン除去食で改善を認める。
- 分子遺伝学的検査でセリアック病関連HLAアレルが検出されなかった患者では、症候の他の原因を精査する必要がある(「鑑別診断」の項を参照)。
グルテン除去食を行っている有症状患者
グルテン除去食を行っている患者ではセリアック病特異的抗体検査は有用ではない。通常はこれらの抗体はもはや存在しないためである。セリアック病の診断を行いたいのであれば、セリアック病の血清検査や小腸生検を行う前にグルテン負荷試験(少なくとも週2回グルテンを含んだ食事をとる)を行ってもよい。
リスクや腸管損傷のため患者がグルテン負荷試験を希望しない場合には診断を確定することはできない。診断を確定するのは控え、症状が軽快しているのであればグルテン除去食を継続する。この場合、分子遺伝学的検査によりセリアック病に対する疾患感受性についての情報を得ることができる。
分子遺伝学的検査でセリアック病関連HLAアレルを調べ、認めない場合にはセリアック病を除外することができ、また認める場合には同疾患に対する感受性があると判断できる。
セリアック病に進展するためには、ヒト白血球型抗原(HLA)クラスⅡ遺伝子HLA-DQA1およびHLA-DQB1の特異的な変異が存在しなければならない。これらの2つの遺伝子はともにセリアック病関連ヘテロ二量体蛋白DQ2・DQ8のα鎖・β鎖をコードしている。
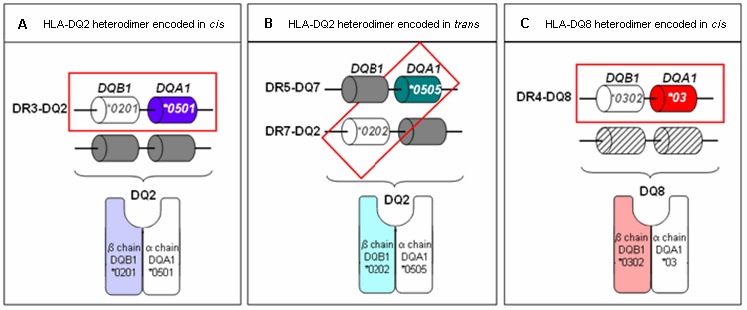
図1
DQ2・DQ8 Aの構造
- DQ2分子は、同じ親の染色体上のHLA-DQA1*0501アレルによりコードされるα鎖蛋白とHLA-DQB1*0201アレルによりコードされるβ鎖蛋白によって構成される(すなわちシス型配置である)。
- DQ2分子は、それぞれの親の染色体上のHLA-DQA1*0505アレルによりコードされるα鎖蛋白とHLA-DQB1*0202アレルによりコードされるβ鎖蛋白によって構成される(すなわちトランス型配置である)。
- DQ8分子は、同じ親の染色体上のHLA-DQB1*0302アレルによりコードされるβ鎖蛋白とHLA-DQA1*03アレルによりコードされるα鎖蛋白によって構成される(すなわちシス型配置である)。
注:DRアレルは連鎖不平衡の結果であり、図だけに記載している。
LM Sollid氏の許諾を得て一部を修正・加筆し掲載。
どの検査方法を用いても、HLA-DQA1およびHLA-DQB1ジェノタイプはセリアック病関連アレルの有無を同定することができる。
以下のいずれかの結果が得られた場合、セリアック病を発症しやすい傾向にある。
- DQ2-陽性(HLA-DQA1*0501/*0505かつHLA-DQB1*0201/*0202)
- 半分のDQ2-陽性(HLA-DQA1*0501/*0505もしくはHLA-DQB1*0201/*0202)
- DQ-8陽性(HLA-DQA1*03かつHLA-DQB1*0302)
セリアック病の発症にはこれらのHLAアレルの存在は必要であるが十分ではない。
- DQ2はセリアック病患者の90%超、および一般人口の20-30%に認められる。
- 少数のセリアック病患者はHLA-DQA1シークエンス変異(*0501もしくは*0505)およびHLA-DQB1シークエンス変異(*0201もしくは*0202)のいずれかを有するが、両方は有さない(すなわちDQ2ヘテロ二量体の半分のみ)。
- DQ8はセリアック病患者の5-10%、および一般人口の約10%に認められる。
分子遺伝学的検査結果の解釈 一般人口の30%はセリアック病関連HLAアレル(ヘテロ二量体DQ2および/もしくはDQ8をコードする)の一つを有し、ヘテロ二量体の1つ、もしくは双方を有する者のわずか3%しかセリアック病を発症しないため、セリアック病関連HLAアレルの同定で診断はできない。
注:食事中のグルテンの存在に検査の信頼性が左右される抗体検査や小腸生検とは異なり、分子遺伝学的検査によるセリアック病関連HLAアレルの結果は、食事とは関係なく正確に解釈することができる。
- 特異的HLA-DQ2/DQ8ジェノタイプに関連するセリアック病の遺伝的リスクを評価することが可能である(表3)。
注:実際のセリアック病のリスクは、セリアック病の症候、セリアック抗体検査陽性、腸生検で陽性所見、家族歴な - その他の因子の存在によって表3で示されたよりもはるかに高い可能性がある。
- いずれのセリアック病関連HLAアレル(表3を参照)を認めない場合、基本的にセリアック病は除外される。
表3 HLA-DQ2および/もしくはDQ8ジェノタイプの結果による遺伝リスク
| HLA DQ2/DQ8 ジェノタイプ1 | リスク1 |
|---|---|
| DQ2+DQ8 | 1:7(14.3%) |
| DQ2+DQ8 もしくは DQ2 DQB1*02ホモ接合 | 1:10(10%) |
| DQ8+DQ82 | 1:12(8.4%)2 |
| DQ8+DQB1*02 | 1:24(4.2%) |
| DQB1*02ホモ接合 | 1:26(43.8%) |
| DQ2単独 | 1:35(2.9%) |
| DQ8単独 | 1:89(1.1%) |
| 一般人口のリスク | 1:100(1%) |
| 1/2 DQ2: DQB1*02 | 1:210(0.5%) |
| 1/2 DQ2: DQA1*05 | 1:1842(0.05%) |
| HLA-DQA/DQBセリアック感受性アレルを認めない | 1:2518(0.04%未満) |
- DQ8+DQ8を除く全てのジェノタイプについてはMeiorniらの文献[2009]による。
- Pietzakらの文献[2009]による。
セリアック関連抗体検査結果が境界域もしくは不明確な有症状患者
以前に施行していないのであれば、tTG, EMA, DGPs IgAおよびIgG, 総IgAを検査するべきである。
セリアック病関連抗体検査が境界域もしくは不明確であり続ける患者では、セリアック病を除外もしくは疾患感受性を評価するため、セリアック病関連HLAアレルの分子遺伝学的検査を行うことを推奨する(「グルテン除去食を行っている有症状患者」「分子遺伝学的検査」の項を参照)。
セリアック病関連HLAアレルを有する患者やグルテンを含有している食事(1日2スライスのパンを2週間以上に相当する)によって臨床的に強く疑われるときには小腸生検が推奨される。
セリアック病の診断は、小腸生検で陽性所見が得られ、グルテン除去食で臨床的/組織学的な改善が認められたときに確定する。
小腸生検の結果が境界域もしくは不明確な有症状患者
病理標本は消化器病理の専門家に評価してもらうべきである。
セリアック病関連HLAアレルの分子遺伝学的検査も有用である(「グルテン除去食を行っている有症状患者」「分子遺伝学的検査」の項を参照)。セリアック病関連HLAアレルを有する患者では、適応があるならば小腸生検に続いてセリアック病関連抗体検査(TTGおよび/もしくはDPGs/EMA)を繰り返し提出すべきである。
セリアック病関連HLAアレルの有無にかかわらずセリアック病関連抗体検査(すなわちTTGもしくはDPGs/EMA)が陰性だった患者では、症候の他の原因の精査を行う(「鑑別診断」の項を参照)。
グルテン除去食が有効ではない有症状患者
注:グルテン除去食を順守しているにもかかわらず症状が続く患者はセリアック病ではない傾向がある。
診断の確認のため、(施行済みであれば)グルテン除去食開始前の初期のセリアック病関連抗体検査結果の見直し、および(施行済みであれば)消化器病理学の専門家による初期の生検標本の再検討が提唱されている。もし結果が否定的であるか結論を出すに至らない場合には、以下が推奨される。
- セリアック病に対するHLA感受性を評価するため、セリアック病関連HLAの分子遺伝学的検査を施行する(「グルテン除去食を行っている有症状患者」「分子遺伝学的検査」の項を参照)。
- セリアック病以外の症候の他の原因を精査する(「鑑別診断」の項を参照)。
- 栄養士に依頼し、気付かずにグルテンを含む食事を摂取していないか、グルテン除去食の効果が乏しくなる乳糖/果糖不耐症がないか評価してもらう。
難治性スプルーが疑われる場合
以下を施行する。
- 免疫組織化学検査で異常な上皮内リンパ球を評価する。
- クローナルT細胞受容体(TCR)遺伝子再構成の解析
- 必要であればT細胞リンパ腫の評価(「セリアック病の病型」「難治性スプルー/セリアック病」も参照)
- 良性および悪性合併症の画像評価。
セリアック病の診断・治療はなかなか筋書きどおりにはいかないが、難治性スプルーも含めてHoffenbergら[2014]によってレビューされている。
セリアック病を合併することが知られる疾患の患者
注:疾患には、ダウン症候群、ターナー症候群、選択的IgA欠損症、自己免疫疾患(インスリン依存性糖尿病、シェーグレン症候群、甲状腺炎)などがある。Guandalini [2004]がレビューしたように、これらの疾患は一般人口よりも高い確率でセリアック病を合併する(「発生率」の項を参照)。
セリアック病特異的抗体検査が推奨される。
セリアック病関連HLAアレルの分子遺伝学的検査にて同アレルを有さない場合には、セリアック病は除外されると考えられている。(「グルテン除去食を行っている有症状患者」「分子遺伝学的検査」の項を参照)
不妊症の女性
未診断のセリアック病は不妊症のリスクとなるため、ほかの原因が除外されている不妊症の女性に対してセリアック特異的抗体検査が考慮されることがある。グルテン除去食は女性患者の妊孕性に対して良い効果をもたらす可能性がある。臨床的特徴
セリアック病や徴候に関する詳細なレビューはGreen & Cellier [2007]やGuandalini & Assiri [2014]の文献を参照されたい。
臨床像
以前には主に吸収不良を起こす消化器疾患と考えられていたが、現在では消化器症状やきわめて多彩な非消化器症状(図2を参照)を呈する全身性の自己免疫疾患として知られている。遺伝的に疾患感受性のある患者では食物中のグルテンによって誘発される。
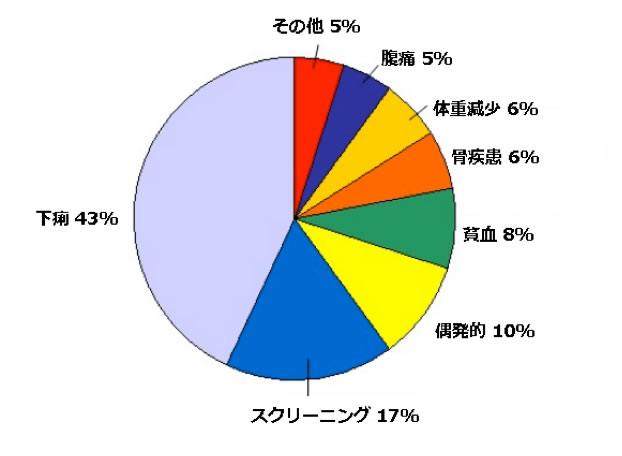
図2
セリアック病の初発症状。初発症状はセリアック病の診断につながる主な症状もしくは兆候である。"骨疾患"は骨密度の低下をさす。"偶発的"とは、通常はセリアック病に関係のない徴候や症状のために行った内視鏡によって、絨毛萎縮が発見されたことを意味する [Green & Jabri 2003, Loら 2003]。
許可を得て転載。
セリアック病は、離乳後のどの年齢でも発症することがある。成人では、診断時年齢のピークは30~50歳である。
症状出現から診断までの平均期間は11年である。他疾患と共通する非特異的症状の範囲が広く、発症年齢もきわめて幅があり、一定の患者は症状を認めない(無症候性すなわちセリアック病)ためである。症状出現と診断までの期間の範囲も、疾患の認知度や患者の臨床所見によって異なる。
診断されたセリアック病の男女比は1:3と報告されている。
セリアック病の症状
セリアック病の症状は多岐にわたり、患者間で大きく異なることが特徴である。主な初発症状の割合については図2を参照されたい。
セリアック病の臨床型は以下に記述するとおりであるが、それだけに限らない。
- 消化器症状 慢性もしくは反復性の下痢、吸収不良、腹痛、腹部膨満、鼓腸、嘔吐、体重減少を認める。患者はしばしば過敏性腸症候群(IBS)と診断されている。50%ものセリアック病患者は診断時に日中の下痢を認めていない。さらに、多くは過体重で、肥満さえ認められる。
- 非消化器症状 ヘルペス様湿疹、慢性疲労、関節痛/関節炎、鉄欠乏性貧血、片頭痛、抑うつ、注意欠陥性障害、てんかん、骨粗鬆症/骨減少症、不妊/習慣流産、ビタミン欠乏、低身長、成長障害、思春期遅発症、エナメル質異常、神経症状、およびさまざまな二次性自己免疫性疾患。
セリアック病の病型
古典的セリアック病とは、下痢・成長障害・体重減少といった吸収不良による軽度~重度の症状が存在することをさす。古典的セリアック病患児は、典型的には生後6ヶ月~2歳の間に発症する。
非古典的セリアック病とは、目立った消化器症状もしくは吸収不良(図2参照)を認めないセリアック病をさす。しかし、非定型セリアック病患者でも逆流症、腹痛、鼓腸、嘔吐、便秘、消化不良などを呈し、しばしば過敏性腸症候群と間違われる。患者の約70%はセリアック病に合併する腸管外症状によって診断される。
鉄欠乏性貧血は非古典的セリアック病の最もよく認められる症状で、かつ唯一の所見である可能性がある。
ヘルペス様湿疹は四肢伸側面の激しい痒みを伴う発疹で、よく認められる非消化器症状である。
その他の腸管外症状には、骨粗鬆症/骨減少症、エナメル質形成不全、不妊/習慣流産、ビタミン欠乏症、トランスアミナーゼ上昇、倦怠感、精神症状や、末梢性ニューロパチー、失調症、痙攣、片頭痛、注意欠陥多動性障害(ADHD)、学業不振をなどさまざまな神経疾患がある。
非古典的セリアック病は通常小児期後期もしくは成人後に発症する。非古典的セリアック病患児は、原因不明の低身長、神経症状、思春期遅発症で発症することがある。
非古典的セリアック病は古典的セリアック病よりも多く認められる。
無症候性セリアック病(silent celiac disease) 無症候性セリアック病は、スクリーニングのセリアック関連抗体検査は陽性で小腸生検にて絨毛萎縮を認めるが症状を欠くものと定義される。無症候性セリアック病患者と判明する場合でもっとも多いのは、家族が罹患者である、もしくはスクリーニング検査である。
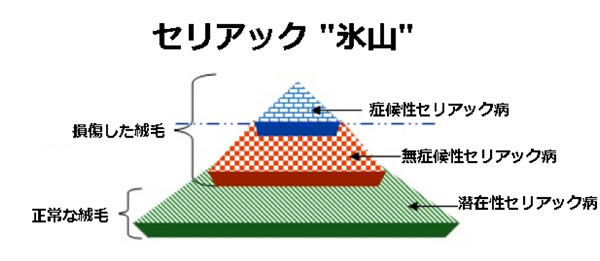
図3
セリアック"氷山"は、遺伝的にセリアック病に罹患しやすい者および関連抗体検査結果が陽性であった者全員を表している。それらのうち多くは潜在性セリアック病患者である。セリアック病の臨床症状を呈する少数は"氷山の一角"である。
潜在性セリアック病 潜在性セリアック病は、血清学的に陽性だが小腸生検は正常であったものと定義される。その患者の一部は、グルテンを摂取し続ければ絨毛萎縮が認められるようになる。
難治性スプルー/セリアック病(RCD) 難治性スプルーもしくは難治性セリアック病は、持続的な腸管の炎症や絨毛萎縮を伴い、厳格なグルテン除去食を少なくとも6~12ヶ月継続したにもかかわらず吸収不良による症状が続いていることをさす。難治性スプルー患者はすべて20歳を超えている。特徴がはっきりしている難治性スプルー患者の文献報告はわずかしかない。予後ははっきりとは分かっていないが、一部の患者はコルチコステロイドや免疫抑制剤が有効である。
- 原発性難治性スプルーは、全くグルテン除去食の効果を認めない状況をさす。主な診断基準の一つとなっているグルテン除去食が有効でないため、分子遺伝学的検査を行うことが重要である。
- 続発性難治性スプルーは、完全に回復した後、グルテン除去食を行っているにもかかわらず再燃を認める状況をさす。
ほかの難治性スプルー/セリアック病(RCD)の分類には、上皮内リンパ球(IELs)で行うものがある。
- 活動性で合併症のないセリアック病では、上皮内リンパ球は表面にCD3およびCD8を発現しているのが普通である。くわえて、これらのリンパ球はクローン的に制限されていない(すなわちポリクローナルである)。
- RCD1では、上皮内リンパ球は正常である。
- RCD2では、上皮内リンパ球は以下のような異常所見を示す。
- 表面のCD3, CD8およびT細胞受容体(TCR)の発現を認めない。
- CD3を細胞内に認める。
- 概してクローン性となっている。
RCD2は免疫抑制剤への反応が悪く、高率に腸管症関連T細胞リンパ腫(EATL)に進展するためRCD1よりも予後は悪い。難治性スプルー患者におけるEATLのリスクは50%を超える可能性がある。
遺伝子型と臨床型の関連
HLA-DQ2および/またはDQ8ジェノタイプの結果による遺伝リスクについては表3を参照のこと。
DQ2およびDQ8双方を有する者の遺伝リスクはもっとも高い。
HLA-DQ2ジェノタイプのみを有する患者とHLA-DQ8ジェノタイプのみを有する患者の間で、セリアック病の臨床的重症度に違いは認められていない。
DQ2とHLA-DQB1*02アレルのホモ接合体を有する者は、DQ2と1つのHLA-DQB1*02アレルを有する者よりもセリアック病のリスクは高い(表3)。
HLA-DQB1*02アレルのホモ接合体は、非古典的セリアック病患者、および難治性スプルーや腸管症関連T細胞リンパ腫(EATL)を含めた重症例よりも古典的セリアック病患者での報告が多い。
DQ2分子の半分(すなわちHLA-DQA1シークエンス変異[*0501もしくは*0505]のみ、もしくはHLA-DQB1シークエンス変異[*0201もしくは*0202]のみ)を有する者がセリアック病を発症することはありうるが、そのリスクは完全なHLA-DQ2ジェノタイプ(すなわちHLA-DQA1シークエンス変異[*0501もしくは*0505]とHLA-DQB1シークエンス変異[*0201もしくは*0202]の両方)を有する者よりはるかに低い。
浸透率
セリアック病の浸透率は低い。セリアック関連HLAアレルジェノタイプを有する者のうち、セリアック病を発症するのは約3%である。「検査戦略」「グルテン除去食を行っている有症状患者」「分子遺伝学的検査」の項と表3を参照されたい。家族のリスクに関しての詳細は「遺伝カウンセリング」の項を参照のこと。
家系内でセリアック病患者が集積していることが示しているように、HLA-DQ2および/またはDQ8ジェノタイプを有する者において、浸透率に対するその他の遺伝的な影響は明らかに存在する。以下の違いが浸透率に影響すると考えられている。
・腸管の透過性 セリアック病患者では、健常人と比較して腸管の透過性は亢進しており、おそらく粘膜下層により多くのグリアジンペプチドが侵入する。ゾヌリン(Zonulin)はタイトジャンクションに関与している蛋白で、セリアック病患者では持続的に上方制御されて傍細胞透過性は亢進するが、健常人ではこの効果は限定的で一過性である。
・グリアジンに対する自然免疫応答 一部の者において、グリアジンに対する自然免疫応答の遺伝的差異はHLA関連免疫応答とは独立してセリアック病や絨毛萎縮の進展に寄与するようである。
発生率
セリアック病の発生率および疫学はGuandaliniら[2014]によってレビューされている。
かつてはまれであると考えられていたが、現在セリアック病は米国人の約1%が罹患していることが知られている。しかし、2012年の全国調査では、セリアック病患者のわずか17%しか診断されていないと推定された。アイルランドやフィンランドで行われたように、医師へのさまざまな臨床症状に関する教育や、セリアック病関連抗体検査の診断への使用により、診断率を上昇させることができる。フィンランドの一部の地方では、セリアック病であることが予測された一般人口の1%のうち、最大70%が同疾患であると診断された。
米国からの報告によると、既知のリスク因子を認めない群におけるセリアック病の全発生率は133人に1人(0.8%)であったが、第一度近親者では22人に1人、第二度近親者では39人に1人、消化器症状もしくはセリアック病に関連する腸管外疾患のいずれかを有する者では56人に1人であった。
tTG IgA検査を用いて、Hoffenbergら[2003]はコロラド州デンバーの5歳児のセリアック病発生率は一般人口の104人に1人であることを報告した。
欧州、米国、豪州、メキシコや南米の一部の国ではセリアック病はよく認められる疾患と考えられている。インド北西部でも報告されている。報告されているなかで最も高いセリアック病の発生率は北アフリカの難民の5.6%である。
アフリカ系カリブ人やアフリカ系アメリカ人においてセリアック病は報告されているが、サハラ以南のアフリカ人でセリアック病と診断されることはまれである。彼らやその他の少数民族における未診断率は高い可能性がある。
以下の疾患ではセリアック病の発生率は高い。
- ダウン症候群(セリアック病の発生率:5~12%)
- ターナー症候群(~3%)
- ウィリアムス症候群(3~10%)
- 選択的IgA欠損症(~2-10%)
- 以下のような自己免疫疾患
- インスリン依存性糖尿病(~6%)
- シェーグレン症候群(~5%)
- 甲状腺炎(~2%-4%)
難治性スプルーの発生率は不明である。おそらくかなり稀である。
遺伝学的関連(アレル)疾患
セリアック病やその合併疾患、および続発性自己免疫疾患の広範囲で多岐にわたる症状以外に
セリアック病関連HLAアレルとの相関は報告されていない。
鑑別診断
症状は多様性に富み、しばしば微細であるため、また他の疾患と臨床像が重複するため、セリアック病は過小診断されている。
セリアック病と紛らわしく誤りやすい疾患には、ディスペプシア、過敏性腸症候群(IBS)、炎症性腸疾患(IBD)、熱帯性スプルー、便秘症、慢性疲労、さまざまな神経疾患などがある。これらのうちの一部はセリアック病を合併することがある。
セリアック病患者のうち当初過敏性腸症候群と診断されていた者は36%に上ると推測される。IBS患者の約5%およびIBD患者の2%はセリアック病も罹患している。
セリアック病以外のグルテン過敏症の原因 グルテン除去食が有効である者の数は、予想されるセリアック病患者の数よりもかなり多いことがますます明白になってきている。
(Saponeら[2012]によってまとめられた)グルテン関連疾患の新しい命名法・分類法によると、発症機序によってグルテン関連疾患は以下の3つに分類される。
- 自己免疫(セリアック病、ヘルペス様湿疹、グルテン失調症)
- アレルギー(小麦アレルギー)
- 免疫介在性、ただし非自己免疫性・非アレルギー性(非セリアック、非アレルギー性グルテン過敏症)
小麦アレルギーは小麦に含まれる蛋白質に対する有害な免疫(アレルギー)反応で、抗小麦IgE抗体の産生を特徴とする。
小麦アレルギーは以下に分類される。
- 古典的食物アレルギー
- 小麦依存性運動誘発アナフィラキシー(WDEIA)
- 職業性喘息(粉屋喘息)および鼻炎
- 接触性蕁麻疹
小麦アレルギーはLevy & Levy-Carrick[2014]によってレビューされている。
小麦アレルギーの診断には皮膚プリックテスト、in vitro IgE検査、経口負荷試験が用いられる。
米国における小麦および/もしくはグルテンアレルギーの発生率は0.4%と報告されている。
非セリアック・非アレルギー性グルテン過敏症 はセリアック病とは異なる疾患だが、グルテン除去食で改善を認めるグルテン過敏症である。非セリアック・グルテン過敏症患者はグルテン不耐性であるが、セリアック病の組織所見(腸生検による特徴的な所見など)もしくはセリアック病特異的抗体(tTGもしくはEMA IgAなど)の上昇は認めない。一部で抗天然グリアジンIgA抗体(AGA)が上昇していることがあるけれども、非セリアック・非アレルギー性グルテン過敏症に特異的な診断マーカーは存在しない。本疾患は、グルテン除去食で改善を認めること、およびセリアック病や小麦アレルギーの除外によって診断される。
非セリアック・グルテン過敏症は(IBSを含めた)消化器症状やセリアック病と同じような腸管外症状で発症することがある。神経/消化器症状を伴い、セリアック病ではないがグルテン除去食で改善を認める者は、評価が難しく、"グルテン過敏症"もしくは"グルテン不耐症"の診断を受けている可能性がある。
グルテンへの病的反応は、セリアック病と非セリアック・グルテン過敏症では異なる。セリアック病は獲得免疫応答によって起きるのに対し、非セリアック・グルテン過敏症は自然免疫応答によって起きると考えられている。
セリアック病と診断された患者1人当たり非セリアック・グルテン過敏症患者は6-7人と推測されている。
臨床的マネジメント
初期診断後の評価
セリアック病と診断された患者における疾患の広がりを把握するために、以下の評価が推奨される。
- グルテンを含有する食事によって診断された患者において、小腸生検を行い絨毛萎縮の程度を評価する(表1)。しかし、絨毛萎縮の程度は臨床所見とは相関しない。
- 成人では、骨粗鬆症/骨減少症を評価するためベースラインの骨密度測定を行う。骨粗鬆症患者では、ビタミンDや副甲状腺ホルモン濃度を測定すべきである。
- 貧血、肝機能異常、栄養障害(鉄・カルシウム・ビタミンD・ビタミンB12・葉酸)のスクリーニング検査を行う。
- 有症状かつ/もしくは高齢の患者では、悪性腫瘍もしくは自己免疫疾患の合併を評価する。
病変に対する治療
セリアック病 理想的には、新たに診断された患者の診療は、消化器科医、プライマリケア医、経験豊富な栄養士などからなるチームによってなされるべきである(図4を参照)。
国営支援グループの地方支部は、さらなる医療資源として活用できる[アメリカ国立衛生研究所コンセンサス委員会2005](図4参照)。
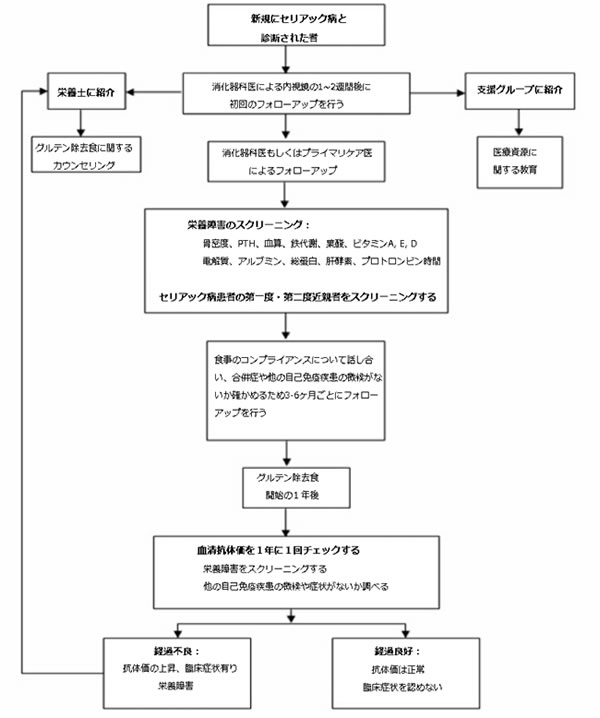
図4
セリアック病と新しく診断された患者の治療アプローチ[Pietzak 2005]
MM Pietzak医師の許可を得て転載
セリアック病患者に対する唯一の治療法は、生涯にわたる小麦・ライ麦・大麦の回避を要するグルテン除去食の徹底である。
- グルテン除去食による治療は腸生検で診断が確定してはじめて開始すべきである。
- セリアック病の経験のある栄養士が参画すべきである。
- 患者の約70%において、グルテン除去食開始後2週間以内に症状は改善する。
- 一部の患者では、ほんの少量のグルテン(すなわち100mg)でも小腸に損傷をきたしうる。パン一切れにおよそ2.5gのグルテンが含まれていることに注意されたい。
- グルテンは多くの食物やそのほかの摂取物に含まれているため、グルテン除去食を徹底することは難しい。密かにグルテンが含まれているものには以下がある。
- 醤油やビールのような非でんぷん質の食料
- 一部の医薬品や化粧品(リップスティックなど)のような食物ではない物質
- 醤油やビールのような非でんぷん質の食料
- 栄養障害や代謝性骨疾患は通常の方法で治療すべきである。
"不応性セリアック病"とは、グルテン除去食で改善を認めないセリアック病をさす。
- 不応性セリアック病でもっともよくみられる原因は、食事中に少量のグルテンが存在していることである。このグルテン摂取は、社交行事での"出来心"や聖餐用聖餅(communion wafers)のような意図的なものから、薬剤中のグルテンやレストランでのグルテンを含む食事を意図せずに摂取する場合まである。良い結果を得るためには、グルテン除去食に精通した栄養士から助言を受けることが推奨される。
- グルテン除去食への反応を悪くすることがあるため、乳糖もしくは果糖不耐症の評価が重要である。
- グルテンの混入では説明のつかない患者では、顕微鏡的大腸炎、膵外分泌機能不全、IBS、小腸内細菌異常増殖(SIBO)、摂食障害など他疾患の存在や合併の評価が必要である。
グルテン除去食に不応である患者では、セリアック病感受性HLAハプロタイプの同定を行うことで、除去食を継続する、グルテンの隠れた供給源を探す、難治性スプルーの可能性を考慮する、あまつさえセリアック病より診断を変更するといった行動につながることがある。
難治性スプルー/セリアック病 グルテン除去食の徹底にもかかわらず症状や腸管の炎症が持続する患者では、全身性の副腎皮質ステロイド(局所活性化型のブデソニドなど)や免疫抑制剤の投与による治療を行う必要があるかもしれない。
一次症状の予防
「病変に対する治療」の項を参照。
母乳栄養は小児期早期にセリアック病の発症に対して防護的な効果があると考えられてきた。しかし、最近の2つの臨床試験ではその事実はないことが示されている。
母乳栄養児と非母乳栄養児を比較したさらに以前の研究では、セリアック病を発症した母乳栄養児は以下のような傾向があることが示された。
- 発症時期がより遅い。
- 下痢、成長障害、嘔吐、腹痛、腹部膨満といった古典的な症状に乏しい。
- "非古典的"な症状の割合が高い。
二次合併症の予防
グルテン除去食による治療によって、
- セリアック病患児の成長障害や骨のミネラル化障害を改善できる。
- 女性患者の自然流産率や低出生体重児の頻度を減少させることができる。
- 小腸腺癌、食道癌、非ホジキンリンパ腫を含むある種の癌のリスクを一般人口レベルに減少させることができる。
- 有症状患者の過度な死亡リスクを減ずることができる。
定期検査
セリアック病患者において血清学的異常は正常になるまでフォローすべきであるが、通常は厳格なグルテン除去食を開始して6~12ヶ月以内にみられる。
腸絨毛の治癒を確認するため、フォローアップ生検を考慮すべきである。厳格なグルテン除去食を行っている患者の一部は徐々に回復するため、生検は典型的には最初の診断から少なくとも2年後に行うべきである。
分子遺伝学的検査でHLA-DQ2もしくはHLA-DQ8セリアック病感受性ハプロタイプを有し抗体は陰性である無症状の親族は、セリアック病関連抗体上昇のスクリーニングのためtTG IgA検査を3~5年おきに施行すべきである。
避けるべき薬物/環境
食物中のグルテンを避ける(「病変に対する治療」および「一次症状の予防」の項を参照)。
リスクのある親族の検査
セリアック病患者の第一度近親者に対する分子遺伝学的検査により、同疾患に罹患しやすく血清スクリーニング検査が有用である者を見出すことができる。第一度近親者は、分子遺伝学的検査を考慮するのに症状を有している必要はない(「検査戦略」「グルテン除去食を行っている有症状患者」「特異的セリアック病関連抗体検査」を参照)。
早期の診断およびグルテン除去食治療により二次性の合併症を予防することができる。
- セリアック病関連HLAアレルDQ2およびDQ8を有さない者は同疾患の血清スクリーニング検査を行う必要はない。
- セリアック病関連HLAアレル(表3)を有する者は3~5年おきにセリアック病関連抗体検査を施行する。
- セリアック病関連抗体が陽性の場合は小腸生検が推奨される。
- セリアック病の確定診断は、小腸生検で陽性所見を認め、グルテン除去食で臨床的および/もしくは組織学的に改善を認める場合になされる。
遺伝カウンセリング目的のリスクのある親族に対する検査に関する問題については「遺伝カウンセリング」の項を参照のこと。
研究中の治療法
研究中であるセリアック病の治療に関する情報についてはここ(pdf)をクリック。
さまざまな疾患や病態に対する臨床試験に関する情報へアクセスしたい場合にはClinicalTrials.govを参照のこと。
遺伝カウンセリング
「遺伝カウンセリングは個人や家族に対して遺伝性疾患の本質,遺伝,健康上の影響などの情報を提供し,彼らが医療上あるいは個人的な決断を下すのを援助するプロセスである.以下の項目では遺伝的なリスク評価や家族の遺伝学的状況を明らかにするための家族歴の評価,遺伝子検査について論じる.この項は個々の当事者が直面しうる個人的あるいは文化的な問題に言及しようと意図するものではないし,遺伝専門家へのコンサルトの代用となるものでもない.」
遺伝形式
HLA-DQ2ジェノタイプ関連セリアック病感受性は、親のセリアック病感受性HLAジェノタイプに応じて常染色体優性遺伝形式もしくは常染色体劣性遺伝形式で受け継がれる(図5を参照)。
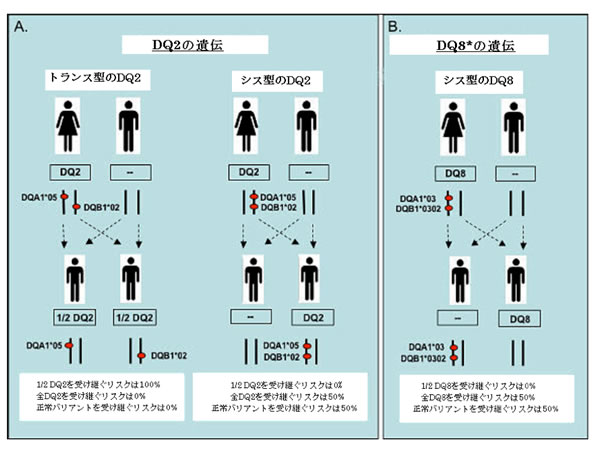
図5
1人の親がセリアック病感受性HLAハプロタイプを有し、他方の親は有さない家系における、A. DQ2関連セリアック病感受性およびB. DQ8関連セリアック病感受性の遺伝形式。連鎖不平衡の結果、シークエンス変異HLA-DQB1*0302は常にシークエンス変異HLA-DQA1*03とともに受け継がれる。
Kimball Genetics, Incにより作成。
HLA-DQ8ジェノタイプ関連セリアック病感受性は常染色体優性遺伝形式で受け継がれる(図5Bを参照)。
患者家族のリスク
HLAが不明で第一度近親者が罹患している者は、セリアック病を発症するリスクは5~20%である。
発端者の両親
- 経験的なデータでは、発端者の両親がセリアック病を発症するリスクは約5~10%であることが示されている。
- DQ2ヘテロ二量体および/もしくはDQ8ヘテロ二量体を有していることが分かっている場合、その親のセリアック病に罹患するリスクは上昇する。DQ2ヘテロ二量体の半分だけ(すなわちHLA-DQA1シークエンス変異もしくはHLA-DQB1シークエンス変異、ただし両方ではない)有している場合、リスクはより小さくなる。
- DQ2セリアック病感受性HLAハプロタイプ(図5Aを参照)もしくはDQ8セリアック病感受性HLAハプロタイプ(図5Bを参照)を有する患者の親は、少なくとも1人はその発端者と同じHLAハプロタイプを有している。
- トランス型のDQ2(図5Aを参照)を有する患者の親はそれぞれ、関連のあるHLAアレルを少なくとも1つ有する。
- DQ2/DQ8関連セリアック病感受性を確認された者はほぼ全員、その親はDQ2/DQ8ヘテロ二量体もしくはDQ2ヘテロ二量体の半分(すなわちDQA1シークエンス変異もしくはDQB1シークエンス変異)を有しているけれども、浸透率の低下、家族が診断されていない、親の発症が遅い、もしくは発症する前に亡くなっているなどで、家族歴はしばしば認めないようにみえる。
発端者の同胞
- HLAハプロタイプが不明である場合、発端者の同胞におけるセリアック病の経験的な全リスクは7~20%である。両親のハプロタイプが分かっている場合は、同胞におけるリスクは絞り込むことができる。
- 発端者と同じセリアック病感受性HLAハプロタイプを共有する同胞は、セリアック病を発症するリスクは40%に達する。
- 発端者の親がシス型のDQ2セリアック病感受性ハプロタイプ(図5Aを参照)もしくはDQ8セリアック病感受性HLAハプロタイプ(図5Bを参照)を有している場合、セリアック病感受性HLAハプロタイプを同胞がそれぞれ受け継ぐリスクは50%である。
- 発端者の片方の親がDQ2ヘテロ二量体の半分(HLA-DQA1*0501もしくは*0505)を有し、もう片方の親がDQ2ヘテロ二量体の半分(HLA-DQB1*0201もしくは*0202)を有する場合、同胞のリスクは以下の通りである。
- 両方のHLAハプロタイプを受け継ぎトランス型の完全DQ2ヘテロ二量体を有するリスク:50%
- DQ2ヘテロ二量体の半分(HLA-DQA1*0501/*0505)もしくは(HLA-DQB1*0201/*0202)を受け継ぐリスク:50%
- HLA-DQA1*0501/*0505もしくはHLA-DQB1*0201/*0202セリアック病感受性ハプロタイプいずれも受け継がないリスク:25%
発端者の子ども
- セリアック病感受性HLAの結果が分からない場合、発端者の子どもにおけるセリアック病の全リスクは5~10%である。子どもがDQ2セリアック病感受性HLAハプロタイプおよび/またはDQ8セリアック病感受性HLAハプロタイプを有している場合、リスクは上昇する。DQ2ヘテロ二量体の半分だけ(すなわちDQA1シークエンス変異もしくはDQB1シークエンス変異、しかし両方ではない)を有する場合、リスクはより低くなる。
- DQ2セリアック病感受性ハプロタイプ(図5Aを参照)もしくはDQ8セリアック病感受性HLAハプロタイプ(図5Bを参照)を有している子どもがセリアック病感受性HLAハプロタイプを受け継いでいる確率はそれぞれ50%である。親と同じHLAハプロタイプを受け継いだ子どものリスクは、発端者と同じHLAハプロタイプを有する同胞よりも低い(すなわち40%未満)。
- トランス型のDQ2セリアック病感受性ハプロタイプ(図5Aを参照)を有する発端者の子どもは、患者である親からセリアック病感受性ハプロタイプの1つを受け継ぐであろう。DQ2/DQ8ヘテロ二量体は一般人口の30-40%に認められるため、発端者のパートナーは検査を受けることがのぞましい。
発端者の他の家族
- 他の家族のリスクは発端者の両親のDQ2/DQ8によって決まる。
- DQ2/DQ8ヘテロ二量体は一般人口の30-40%に認められるため、発端者のパートナーのセリアック病感受性ハプロタイプも重要である。
遺伝カウンセリングに関連した問題.
早期診断・治療を目的としたリスクのある親族の検査についての情報は、「臨床的マネジメント」「リスクのある親族の検査」を参照のこと。
家族計画
- 遺伝的リスクの確認や保因者診断、および出生前診断の利用に関する話し合いを行う最適な時期は妊娠前である。
- 罹患している、キャリアである、もしくはキャリアであるリスクがある若年成人に対し、遺伝カウンセリング(潜在的な子どもへのリスクや出産方法の選択肢に関する話し合いなど)を申し出ることがのぞましい。
DNAバンクは(主に白血球から調整した)DNAを将来利用することを想定して保存しておくものである。検査技術や遺伝子、アレル変異、あるいは疾患に対するわれわれの理解が将来さらに進歩すると考えられるので、患者のDNA保存を考慮すべきである。
出生前診断
技術的には可能であるが、この複雑な疾患におけるセリアック病感受性HLAバリアントの出生前検査はのぞましくない。その理由は以下による。
- 遺伝的変化は一般人口においてもよくみられることである。
- 遺伝的変化はセリアック病の素因にはなるが発症を予測できない。
- 極めて有効な治療法が存在する。
更新履歴
- Gene Reviews著者: K Taylor, MS, PhD, CGC, Benjamin Lebwohl, MD, MS, Cara L Snyder, MS, CGC, and Peter HR Green, MD.
日本語訳者: 和田宏来 (県西総合病院小児科/筑波大学大学院小児科)
Gene Reviews 最終更新日: 2015.9.17. 日本語訳最終更新日: 2017.12.8.(in present)
