歯周型Ehlers-Danlos症候群
(Periodontal Ehlers-Danlos Syndrome)
[Synonyms:EDS Type VIII, pEDS]
Gene Reviews著者: Ines Kapferer-Seebacher, DMD, Fleur S van Dijk, MD, PhD, and Johannes Zschocke, MD, PhD.
日本語訳者: 佐藤康守(たい矯正歯科)、櫻井晃洋(札幌医科大学医学部遺伝医学)
GeneReviews最終更新日: 2021.7.29. 日本語訳最終更新日: 2023.4.7.
原文: Periodontal Ehlers-Danlos Syndrome
要約
疾患の特徴
歯周型Ehlers-Danlos症候群(pEDS)は、口腔に独特の症候が現れることを特徴とする。ティーン世代に始まる歯周組織の崩壊により、歯の早期喪失が生じる。付着歯肉の欠如、ならびに、薄く脆弱な歯肉のため、歯肉退縮が生じる。pEDSでみられる結合組織の異常は、通常、痣のできやすさ(easybruising)、脛骨前部の斑(pretibialplaques)、遠位関節の可動性亢進、嗄声などの形で現れ、それらより少ないながら、臓器破裂や血管破裂がみられることもある。pEDSは、1970年代の最初の報告以降、148人が文献の形で報告されている。しかしながら、今後本疾患の臨床的特徴をさらに明確化していく上では、分子レベルでpEDSの診断が確定した新たな例について、口腔以外の症候を詳細に明らかにしていくことが重要である。
診断・検査
発端者におけるpEDSの診断は、これを示唆する臨床所見を有することに加え、分子遺伝学的検査にてC1RもしくはC1Sに機能獲得型病的バリアントのヘテロ接合が同定されることをもって確定する。
臨床的マネジメント
症状に対する治療:
治療は、現存する臨床症候に基づいて、個別的に行われる。重度の歯周炎が早期から現れる特徴があることから、罹患者は全例、歯周病専門医の診察を定期的に受ける必要がある。また、口腔衛生を常に最良の状態に保つことも、現存する歯周炎の治療上の1つの大きな要素である。歯を失うと、多くの場合、歯槽骨も同時に破壊されてしまうため、補綴作業はかなり難しくなる。関節の可動性亢進に対しては、理学療法、作業療法、疼痛管理、適切な運動が有効である。
定期的追跡評価:
歯周疾患の進行リスクが高いため、歯周組織パラメーターの再評価、口腔衛生指導(例えば、歯間清掃用具や電動歯ブラシ)、歯肉縁上・歯肉縁下の壊死組織除去といった歯周組織支持療法を、個々のニーズに応じ、3-6ヵ月ごとに行うことが推奨される。関節可動性亢進に伴う合併症については、必要に応じ、リウマチ専門医、理学療法士、作業療法士などが対応する。
リスクのある血縁者の評価:
予防的口腔衛生、ならびに通常の歯科的ケアや追跡評価を迅速に開始することによって利益が得られる人をできるだけ早期に特定することを目的として、リスクを有する罹患者の血族に対しては、見かけ上、無症状であっても、また、罹患者より年上であるか年下であるかを問わず、その遺伝学的状態を明らかにしておくことが望ましい。
遺伝カウンセリング
歯周型EDSは、常染色体顕性の遺伝形式をとる。大多数のpEDS罹患者は、片親からC1RもしくはC1Sの病的バリアントを継承して本疾患を有するに至った例である。罹患者の子が病的バリアントを継承し、疾患を発症する可能性は50%である。家系内に存在するpEDSを引き起こす病的バリアントが同定済の場合は、出生前診断や着床前遺伝学的検査を行うことが、技術的には可能である。
診断
2017年版Ehlers-Danlos症候群の疾病分類[Malfaitら2017]において、歯周型Ehlers-Danlos症候群(pEDS)の正式な診断基準が確立されるに至った。
本疾患を示唆する所見
以下のような大基準・小基準の組合せ、ならびに家族歴を有する成人については、歯周型Ehlers-Danlos症候群(pEDS)を疑う必要がある。
臨床所見
大基準
- 早期(小児期あるいは思春期)発症型の重度の歯周炎
- 付着歯肉の全顎的欠如(図1)(付着歯肉の完全欠如は、pEDSの疾患特異的所見と考えることができる[Kapferer-Seebacherら2021])
- 脛骨前部の斑(すなわち、ヘモジデリン沈着)(図2)
- 診断基準を満たす第1度近親が存在するという家族歴(わかっている限り家族歴陰性であったとしても、本疾患の可能性が除外されるわけではない)
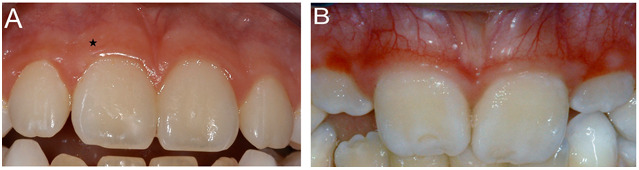
図1:
付着歯肉の全顎的欠如は、歯周型Ehlers-Danlos症候群の大基準の1つである。
A.健常者においては、帯状の厚く角化した歯肉(*)が、機械的な保護の役目を果たしている。付着歯肉はⅠ型コラーゲン線維を通じて骨膜と固く不動性の結合を形成している。
B.歯周型Ehlers-Danlos症候群では付着歯肉が欠如しているため、粘膜が遊離歯肉にまで延びている。
口腔粘膜は非角化性で、骨膜とは緩く結合している。健常者でみられる付着歯肉に比べ、口腔粘膜は薄く脆弱で、血管がはっきり視認できるだけの透明度を有している。
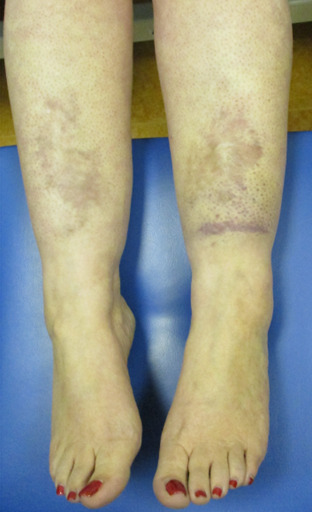
図2:
歯周型EDS罹患者の83%に脛骨前部の斑が報告されている[Kapferer-Seebacherら2016]。茶色味を帯びた脛骨前部の斑の組織学的解析で、皮膚の線維化とヘモジデリン沈着が明らかとなっている[Roncerayら2013]。罹患者の中には、脛骨前部に1回だけ外傷を起こした後、血腫ができて、それがずっと改善しないと訴える例もみられる。
小基準
- 痣のできやすさ
- 目立つ血管
- 主として遠位関節にみられる関節可動性亢進
- ヘルニア
- Marfan症候群様顔貌
- 先端早老症
- 皮膚の過伸展性と脆弱性,異常な瘢痕化(広範囲あるいは萎縮性)
- 感染発生頻度の上昇
pEDSを示唆する最小基準
- 以下の大基準のうちのいずれか1つを有すること
- 重度かつ難治性の早期(小児期あるいは思春期)発症型歯周炎
- 付着歯肉の欠如
- 上記に加えて以下の条件を2つとも満たすこと
- 他の大基準を少なくとも2つ有すること
- 小基準を1つ有すること
pEDSの診断基準[Malfaitら2017]が公表されて以降、pEDSで嗄声、高調の声の報告もみられる[Georgeら2016]。
10歳未満の罹患児に一貫して認められる臨床所見は、付着歯肉の全顎的欠如のみである。したがって、小児の診断に際しては、現行の基準の組合せは必ずしも適したものではない。痣のできやすさと歯肉出血は別として、その他の臨床所見は、幼児期には軽度もしくは欠如する。したがって、10歳未満については、付着歯肉の欠如と第1度近親の家族歴が揃えば、それはpEDSを示唆するものとなりうる[Kapferer-Seebacherら2021]。
画像所見
歯科の画像
- 歯科的スクリーニングとして、パノラマX線写真が挙げられる。
- 歯周組織の診断と治療を目的として、パノラマX線写真に、咬翼法やデンタルX線写真の全顎撮影といった口腔内X線写真を選択的に追加することが考えられる。
成人における脳のMRI
pEDS罹患成人の脳のMRIにて、年齢とともに進行する皮質下小血管の障害を示唆するパターンの白質異常が明らかになることがある。
診断の確定
発端者における歯周型Ehlers-Danlos症候群の診断は、これを示唆する所見を有することに加え、配列解析でC1もしくはC1Sに機能獲得型病的バリアントのヘテロ接合が同定されることをもって確定する(表1参照)。
注:C1RやC1Sに意義不明バリアントのヘテロ接合が同定された場合、それは、本疾患の診断を確定させるものでも否定するものでもない。
分子遺伝学的検査のアプローチとしては、表現型に合わせて、遺伝子標的型検査(マルチ遺伝子パネル)と網羅的ゲノム検査(エクソームシーケンシング,ゲノムシーケンシング)を組み合わせるやり方が考えられる。
遺伝子標的型検査の場合は、臨床医の側で関与が疑われる遺伝子の目星をつけておく必要があるが、ゲノム検査の場合、その必要はない。「本疾患を示唆する所見」に記載した特徴的所見を有する例については遺伝子標的型検査(「方法1」参照)で診断がつく可能性が高いものと思われるが、pEDSを頭に入れるところにまで至らない例については、ゲノム検査(「方法2」参照)で診断がなされることになろう。
方法1
- Ehlers-Danlos症候群用マルチ遺伝子パネル
現況の表現型と直接関係のない遺伝子の意義不明バリアントや病的バリアントの検出を抑えつつ、疾患の遺伝的原因の特定に最もつながりやすいのは、C1RとC1Sを含むEhlers-Danlos症候群用マルチ遺伝子パネルであるように思われる。
注:(1)パネルに含められる遺伝子の内容、ならびに個々の遺伝子について行う検査の診断上の感度については、検査機関によってばらつきがみられ、また、経時的に変更されていく可能性がある。
(2)マルチ遺伝子パネルによっては、このGeneReviewで取り上げている状況と無関係な遺伝子が含まれることがある。
(3)検査機関によっては、パネルの内容が、その機関の定めた定型のパネルであったり、表現型ごとに定めたものの中で臨床医の指定した遺伝子を含む定型のエクソーム解析であったりすることがある。
(4)ある1つのパネルに対して適用される手法には、配列解析、欠失/重複解析、ないしその他の非配列ベースの検査などがある。
マルチ遺伝子パネル検査の基礎的情報についてはここをクリック。
遺伝学的検査をオーダーする臨床医に対する、より詳細な情報についてはここをクリック。
方法2
- 網羅的ゲノム検査
エクソームシーケンシングやゲノムシーケンシングといった網羅的ゲノム検査によってpEDSの診断に至るようなこともある。
網羅的ゲノム検査の基礎的情報についてはここをクリック。
ゲノム検査をオーダーする臨床医に対する、より詳細な情報についてはここをクリック。
表1:歯周型Ehlers-Danlos症候群で用いられる分子遺伝学的検査
| 遺伝子1 | その遺伝子の病的バリアントに起因するpEDSの割合2 | その手法で病的バリアント3が検出される割合 | |
|---|---|---|---|
| 配列解析4 | 遺伝子標的型欠失/重複解析 | ||
| C1R | 90%近く | 100%近く | こうした病的バリアントはないと思われる6 |
| C1S | 10%近く | 100%近く | こうした病的バリアントはないと思われる6 |
- 染色体上の座位ならびにタンパク質に関しては、表A「遺伝子とデータベース」を参照。
- Kapferer-Seebacherら[2016]
- この遺伝子で検出されているバリアントの情報については、「分子遺伝学 」の項を参照のこと。
- 配列解析を行うことで、benign、likelybenign、意義不明、likelypathogenic、pathogenicといったバリアントが検出される。バリアントの種類としては、遺伝子内の小欠失/挿入、ミスセンス・ナンセンス・インフレームのスプライス部位バリアントなどがあるが、通常、エクソン単位あるいは遺伝子全体の欠失/重複については検出されない。ただ、こうしたもの(ナンセンスバリアントやアウトオブフレームバリアントも含めて)でpEDSが生じることはないように思われる。配列解析の結果の解釈に際して留意すべき事項についてはこちらをクリック。
- 遺伝子標的型欠失/重複解析でpEDSを引き起こすバリアントが検出されることはないように思われる。
- Kapferer-Seebacherら[2016],Ballyら[2019],Gröbnerら[2019]
臨床的特徴
臨床像
歯周型Ehlers-Danlos症候群(pEDS)は、独特の口腔症候を特徴とする。歯の支持組織(すなわち、歯槽骨、歯周靱帯、歯根セメント質、歯肉付着)に早発性で重度の破壊が生じることで、歯の早期喪失をきたす。付着歯肉が欠如し、歯肉が薄く脆弱であるため、歯肉退縮が生じることになる。pEDSでみられる結合組織の異常としては、痣のできやすさ、脛骨前部の斑、遠位関節の可動性亢進、嗄声があり、その他の比較的少ない症候としては、臓器破裂や血管破裂がある(表2参照)。
1970年代にpEDSが初めて報告されて[McKusick1972,Stewartら1977]以降、これまでに34の症例報告、7つの血統解析、2つのコホート研究[Kapferer-Seebacherら2017,Wuら2018,Kapferer-Seebacherら2019,Cortés-BretónBrinkmannら2021,Kapferer-Seebacherら2021]の計148人が報告されている。これから述べる本疾患に伴って現れる表現型としての症候は、こうした報告を基礎としたものである。ただ、今後、分子レベルでの診断が確定した新たな例については、口腔以外の症候をさらに詳細に明らかにし、本疾患の臨床症候をいっそう明確にすることが重要であろう。
表2:歯周型Ehlers-Danlos症候群:代表的症候の出現頻度
| 症候 | その症候を有する罹患者の割合 | コメント | |
|---|---|---|---|
| 歯 | 早期発症の重度歯周炎 | 99% | 小児期あるいは思春期に診断がなされる(平均発症年齢14歳) |
| 歯肉退縮 | 成人の98% | ||
| 付着歯肉の全顎的欠如 | 93% | 確認には臨床経験が必要。疾患特異的と思われるが、pEDS罹患者でこれが漏れなく評価・報告されていない現状がある。 | |
| 痣のできやすさ | 96% | 主として脛であるが、変わった部位(例えば、頰や大腿)に現れる場合もある。 | |
| 脛骨前部の斑 | 83% | 脛骨前部の(ヘモジデリン)変色として報告されているものもある。 | |
| 皮膚の脆弱性,萎縮性瘢痕,創傷治癒の遅延 | 50% | ||
| 関節可動性亢進 | 44% | 以前は、主として小関節に生じると報告されていた。 | |
| 動脈瘤/動脈解離 | 145人中8人 | 腹部大動脈(n=2),頸動脈(2),脳動脈(3),部位不明(1) | |
| 脳白質の異常 | 8人中8人 | 脳のMRIを行った成人の全例で報告されている。 | |
| 臓器破裂 | 145人中2人 | 肺,横隔膜,腸,小腸,鼓膜 | |
Kapferer-Seebacherら[2016],Kapferer-Seebacherら[2017]を基に集計。
歯の所見
早期発症型歯周炎
早期発症型の歯周炎が、pEDSでみられる主たる症候である。
早期発症型歯周炎が罹患成人の98.4%で報告されている[Kapferer-Seebacherら2017]。ただ、今のところpEDSの歯周組織や歯の特徴に関するデータは不足している。pEDS罹患者ではあるが、血縁者内でただ1人だけ歯周炎を有していないという成人の例が複数確認されている。これらの例はいずれも、付着歯肉の全顎的欠如、脛骨前部の斑、pEDSの家族歴があり、臨床診断基準を満たしていた。
歯周炎発症年齢の中央値は14歳(範囲:2-35歳)と報告されている[Kapferer-Seebacherら2016]。ただ、このデータは、後ろ向きに収集したデンタルX線写真、あるいは罹患者自身の回想(例えば、歯周組織が原因で最初に歯を喪失したと自身が記憶している年齢)に基づくものなので、あくまで大まかな推定値と考えるべきものである。
12人の罹患児(8-13歳)を対象とした臨床研究で、最年長の例(13歳)のみが最大6mmの歯槽骨の喪失を示した。これは、歯周炎の発症を主として思春期とする考え方を裏づけるものとなっている[Kapferer-Seebacherら2021]。付け加えると、「歯が根ごと抜けた」と親が言うように、3,4歳の段階で乳歯が早期喪失をきたした報告もみられる。これは、乳歯の歯周炎に起因するものであるように思われる。
大多数の罹患者は歯磨き時の出血を訴えるが、歯肉出血の頻発(これは歯肉炎の1つの徴候)は主観的なもので、また、一般集団でもプラークコントロール不良例では非常に多くみられるものであるため、評価の難しいところである。
付着歯肉の全顎的欠如
口腔組織の脆弱化につながる付着歯肉の欠如あるいは減少は、1995年に初めて報告されたものであるが[Cunniff&Williamson-Kruse1995]、pEDSだけにみられる疾患特異的所見であるように思われる。
健常者の歯肉は、角化性の付着歯肉と、非角化性で可動性の口腔粘膜とに分けられる。角化した付着歯肉は、Ⅰ型コラーゲン線維を介して骨膜と固く不動性の結合を形成し、分厚い帯として機械的な保護機能を果たす。それに対し、角化していない口腔粘膜は薄く、より脆弱で、透明感があり、骨膜とは疎な結合を示すのみである。pEDSにおいては、厚い帯状の歯肉が失われてしまっており、脆弱な粘膜が歯肉縁に達する。そのため、組織は脆くなり歯肉退縮を起こしやすくなる。
全顎的歯肉退縮
成人のpEDS罹患者の87.1%に全顎的歯肉退縮が報告されている。これは、付着歯肉の欠如、ならびに歯周組織の付着の進行性喪失に起因するものである。
Ehlers-Danlos症候群の所見
痣のできやすさ
pEDSのほぼ全例(96%)で、幼児期以降、脛骨前部を中心とした痣のできやすさが報告されている[Kapferer-Seebacherら2016]。痣のできやすさは、主観的、非特異的性格をもつため、評価の難しいところであるが、湯でシャワーを浴びた後やスポーツの後に、頰や大腿といった、ふつう痣のできない部位に痣ができることがある[Kapferer-Seebacherら2019]。
脛骨前部の斑
茶色味を帯びた脛骨前部の皮膚の組織学的分析により、皮膚線維症とヘモジデリン沈着が明らかとなっている[Roncerayら2013]。罹患者の中には、過去に1度脛骨前部の外傷があって血腫ができた後、それがずっと治らずにいると報告する人もいる。古典型、血管型、関節可動亢進型の各タイプのEDSとは異なり、pEDSでみられる脛骨前部の斑は、多くの場合、類壊死状で、結合組織のマトリックスの炎症や変性がより重度であることを反映したものとなっている[Georgeら2016]。
皮膚の脆弱性,萎縮性瘢痕,創傷治癒の遅延
皮膚の脆弱性は、脛を中心に、痣のできやすさとして、また、「タバコの巻紙様」瘢痕の形で現れることがある[Georgeら2016]。萎縮性の脛骨前部の斑の内部に、慢性下肢潰瘍が生じることがある[Roncerayら2013]。罹患者家系中で1人だけ、脛骨前部に開放創ができ、治癒に数ヵ月から数年かかった、あるいは皮膚移植を要した例があるとの報告が複数みられる[Georgeら2016,Kapferer-Seebacherら2016]。
関節の可動性亢進
関節可動性亢進は、遠位関節のみに現れることが多い[Kapferer-Seebacherら2016]。
動脈瘤/動脈解離
動脈瘤/動脈解離は、145人のpEDS罹患者中8人で報告されており、特定の家系内に集中する傾向にあるようである。臨床診断がなされた1家系4人の罹患者においては、多様な幅の心血管イベントがみられている。その内容は、大動脈解離(46歳)、突然死(23歳)、脳動脈瘤の出血(42歳)、心臓発作(43歳)であった[Kapferer-Seebacherら2016]。脳動脈瘤については、互いに血縁関係のない別の複数の家系の罹患者でも確認されている[Cıklaら2014,Kapferer-Seebacherら2016]。ただ、動脈瘤・動脈解離のリスクを明らかにするためには、より長期にわたるデータが必要である。動脈瘤・動脈解離のリスクは、血管型EDS罹患者よりは低い模様である。血管型EDSにおいては、72%の罹患者で、1つないしそれ以上の数の血管合併症が報告されている[Frankら2015]。
臓器破裂
罹患者148人中2人(1.4%)で、複数の臓器破裂が報告されている。うち1人は67歳で、反復性気胸、腸穿孔、鼠径ヘルニアを示した[Kapferer-Seebacherら2016]。もう1人のほうは57歳で、肺と横隔膜の破裂を示した[Kapferer-Seebacherら2019]。
その他
先端早老症
pEDS罹患者で、血管型EDSでみられるものを思わせるような手足の先端早老性変化が報告されている[Georgeら2016]。
高調の嗄声
これまでに、pEDSの2例で高調の嗄声が報告されている[Georgeら2016,Kapferer-Seebacherら2019]。声質の異常は他のタイプのEDSでも時に報告されており、声帯靱帯のコラーゲンの異常に起因するものではないかと考えられている[Georgeら2016]。
脳白質の異常
これまでに脳のMRIが行われたすべての成人例で、脳の白質の異常が報告されている[Sprangerら1996,Kapferer-Seebacherら2019]。
MRIのパターンは、背景に、年齢とともに進行する小血管疾患が存在することを示唆するものであった。微小血管障害関連のその他の白質脳症がそうであるように、白質の変化は、神経学的症候が乏しいこととはおよそ不釣り合いなほどに広範なものであった。病歴として、家系内で1人だけ、反復性の頭痛あるいは鬱があるという例が複数みられた。神経学的検査では、軽度の認知機能低下、運動失調、1度の発作歴が1人でみられたものの、他の罹患者は全例、特記事項はなかった。
子どもでみられる臨床症候
現在までに報告されているpEDSの小児例は、1例を除きすべて、陽性の家族歴がきっかけで同定に至ったものである。10歳未満の罹患児に一貫してみられる唯一の臨床所見は、付着歯肉の全顎的欠如である[Kapferer-Seebacherら2021]。
罹患児の親のほうから、例外なく、痣のできやすさや歯肉出血の報告があるものの、子どものpEDS罹患者については、付着歯肉の全顎的欠如以外の臨床症候は、軽度であるか、もしくは全くみられない。歯周炎発症年齢の中央値は14歳と報告されている。
注目すべき古典型EDSの1小児例がある。この例は乳歯列の歯槽骨の欠損を呈し、歯肉の表現型はpEDSのそれであった。COL5A1の家族性の病的バリアントを有していたが、それと同時に、C1Rのdenovoの病的バリアントを併せもっていた[Stockら2021]。
遺伝型-表現型相関
pEDSについては、確認済の遺伝型-表現型相関は存在しない。
浸透率
現時点までに確認されている例では、浸透率は100%である。ただ、年齢が関連する要素もあり、例えば歯周炎などは、口腔衛生の良好な例を中心に、若年時にはみられないこともある[Kapferer-Seebacherら2021]。
疾患名について
歯周型EDSは、もともと、Ehlers-Danlos症候群Ⅷ型と呼ばれていた[Stewartら1977]。Villefranche命名規約[Beightonら1998]で、EDS歯周炎という名称が初めて用いられている。
発生頻度
pEDSの発生頻度に関する推定値は、どの集団の数字も存在しない。
現在までに、34の症例報告、7つの血統解析、2つのコホート研究を合わせ、計148人のpEDS罹患者が報告されている[Kapferer-Seebacherら2017,Wuら2018,Kapferer-Seebacherら2019,Cortés-BretónBrinkmannら2021,Kapferer-Seebacherら2021]。
一般集団における歯周炎の有病率が高いこと[Chenら2021]、ならびに、pEDSでは時に結合組織の症候がごく軽度なものにとどまることがあることから考えて、本疾患については、実際より少ない数しか診断がなされていない可能性があるように思われる。
遺伝学的に関連のある疾患(同一アレル疾患)
補体第1成分サブユニットタンパク質欠損(これは常染色体潜性遺伝形質で、C1s欠損症[OMIM613783]を含む)は、全身性エリテマトーデス(SLE)の表現型を引き起こすことがある。この疾患は、臨床的にも病原の上でもpEDSとは無関係である[Macedo&Isaac2016,Demirkayaら2017]。
鑑別診断
歯周型EDS(pEDS)は、歯周炎その他のpEDS関連症候を呈する遺伝性疾患と鑑別する必要がある。こうした疾患とpEDSとを鑑別する上では、歯肉に現れる表現型、ならびにその発症年齢が有用である。
注:現行の歯周疾患の分類においては、「複雑遺伝疾患としての歯周炎」(すなわち、「後天性歯周炎」)と、「全身疾患(歯周型EDSはここに入る)の1症候としての歯周炎」は区別されている。
遺伝性疾患
表3:歯周型Ehlers-Danlos症候群との鑑別診断に関係してくるような口腔症候を呈する遺伝性疾患
| 疾患名 | 遺伝子 | 遺伝形式 | 症候 | 他の症候 | |
|---|---|---|---|---|---|
| 口腔 | 皮膚 | ||||
| 血管型EDS(vEDS) | COL3A1 | AD (AR) |
歯肉退縮,歯肉の脆弱性,歯肉出血1 vEDSでは早期に重度の歯周炎が生じることはない。 |
外傷以外の出血,ふつうみられない部位の出血 vEDSでは脛骨前部の斑はみられない。 |
動脈瘤/動脈破裂,臓器破裂(vEDSを示唆する動脈瘤や臓器破裂は、pEDSでも報告されてはいるものの、出現頻度はずっと低い);早老を思わせる外観,目立つ眼,垂れていない耳垂、手足の先端早老性変化,小関節の可動性亢進 |
| 遺伝性血管性浮腫 | SERPING1 (C1INH) |
AD AR |
歯槽骨吸収 過去何度かの急性歯肉浮腫の既往 |
急性一過性の血管性浮腫 | |
| 低ホスファターゼ症 | ALPL | AD AR |
乳歯・永久歯の早期喪失 | 反復性骨折;骨軟化症;くる病,血清アルカリホスファターゼの低下,尿中リン酸エタノールアミンの上昇 | |
| Kindler症候群 | FERMT1 | AR | 早期発症の重度歯周炎 | 先天性水疱,皮膚萎縮,光過敏症,脆弱な皮膚 | |
| 歯限局型低ホスファターゼ症(「低ホスファターゼ症」のGeneReviewを参照) | ALPL | AD AR |
乳歯・永久歯の早期喪失 | 血清アルカリホスファターゼの低下,尿中リン酸エタノールアミンの上昇 | |
| Papillon-Lefèvre症候群 (OMIM245000) |
CTSC | AR | 幼児期に発症する重度の歯周炎 | 掌蹠角化症 | |
| 重症先天性好中球減少症 (OMIMPS202700) |
CSF3R ELANE G6PC3 GFI1 HAX1 JAGN1 SRP54 VPS45 WAS |
AD AR XL |
幼児期に発症する重度の歯周炎 | 重度の反復性感染症、血液所見 | |
| Singleton-Merten症候群 (OMIM182250, 616298) |
DDX58 IFIH1 |
AD | 歯の早期喪失,短根 | 低身長,大動脈石灰化,大動脈弁・僧帽弁石灰化,骨粗鬆症 | |
AD=常染色体顕性;AR=常染色体潜性;XL=X連鎖性
- Hartsfield&Kousseff[1990],Pitney&Pitney[2020]
pEDSは、表3にまとめた疾患に加えて、他のタイプのEDSや血管病変を伴う一連の疾患群とも一部の表現型を共有する。しかし、こうした疾患では目立った口腔症候がみられないため、そうしたものとの臨床的鑑別は容易である。具体的には、次のような疾患が挙げられる。
- 古典型EDS,Ehlers-Danlos症候群古典/血管型[Nuytinekら2000,Malfaitら2007],脊椎後側彎型EDS(「KFBP14脊柱後側彎型Ehlers-Danlos症候群」ならびに「PLOD1関連脊柱後側彎型Ehlers-Danlos症候群」のGeneReviewを参照)
- 非症候群性大動脈障害(「遺伝性胸部大動脈疾患概説」のGeneReviewを参照)
- Loeys-Dietz症候群
- 常染色体顕性遺伝性多発性嚢胞腎
- Marfan症候群
歯周炎
歯周炎は、さまざまな環境的病原因子と遺伝的病原因子が組み合わさって相互作用することで、発症時期、疾患の進行、重症度が決まると考えられている多因子疾患である。歯周炎は、細菌性微生物が引き金となって生じ、歯の支持組織(歯槽骨,歯周靱帯,歯根セメント質,歯肉付着)に慢性炎症性の破壊が生じることを特徴とし、進行した例では歯の喪失に至る。歯周炎を定義する上での鍵となるポイントは、臨床の場で歯間部のアタッチメントロスを認めることである[Tonettiら2018]。歯周炎の罹患者は、通常、30歳超で、骨の破壊量は、存在する歯垢や歯石と一致する。疾患の進行速度は、局所的要因、全身的要因、喫煙や感情面でのストレスといった外的要因による修飾を受ける可能性がある。
現行の歯周疾患・インプラント周囲疾患の分類によると、「歯周炎」は、「壊死性歯周疾患」や「全身疾患の1症候としての歯周炎」とは区別すべきものとされている。そして、後者の中には、pEDSのような稀少な全身疾患に伴うものも含まれる[Cartonら2018]。
稀少疾患の1症候としての歯周炎とは対照的に、一般の歯周炎は非常に有病率の高い疾患である。人口ベースの研究によると、歯周炎は、全体の72.4%、うち重度歯周炎(ステージⅢとⅣに相当するもの)が17.5%に上るという[Germenら2021,Stødleら2021]。若年者における歯周炎の有病率は、0.1%(北ヨーロッパ,中央ヨーロッパ起源の人)から5%(アフリカ起源の人)の間である[Albandar2014]。これに対し、pEDSでは成人の98%が歯周炎を有し、主としてステージⅢとⅣに準ずる臨床的/放射線的アタッチメントロスがみられる[Kapferer-Seebacherら2016,Kapferer-Seebacherら2017]。
臨床的マネジメント
今のところ、公表された歯周型Ehlers-Danlos症候群(pEDS)に関する臨床的管理のガイドラインは存在しない。それでも、推奨事項のようなものはいくつか存在する[著者らの個人的見解]。
最初の診断に続いて行う評価
歯周型Ehlers-Danlos症候群と診断された罹患者については、疾患の範囲やニーズを把握するため、診断に至る過程ですでに実施済ということでなければ、表4にまとめたような評価を行うことが推奨される。
表4:歯周型Ehlers-Danlos症候群罹患者の最初の診断後に行うことが推奨される評価
| 系/懸念事項 | 評価 | コメント |
|---|---|---|
| 早期発症型の重度歯周炎/歯肉退縮 | 臨床における歯周組織の検査,歯のX線写真 | 歯周病専門医、あるいは歯周病学を専門とする歯科医師であることが必要。 |
| 痣/瘢痕のできやすさ | 皮膚科医による臨床的評価 | |
| 神経学的症候 | 神経内科指導医による臨床的評価 | 脳のMRI。 臨床的意義の不明な白質異常がこれまでにpEDS罹患者で報告されているため。 |
| 関節可動性亢進 | 臨床的評価 | 通常は、pEDSの診断を行った指導医の手で行われる。 |
| 動脈瘤 | 成人について、動脈樹の画像診断 | |
| 嗄声 | 耳鼻咽喉科での相談 | 臨床的評価を行う。 |
| 遺伝カウンセリング | 遺伝の専門医療職1の手で行う。 | 医学的、個人的な意思決定の用に資するべく、本人や家族に対し、pEDSの本質、遺伝形式、そのもつ意味についての情報提供を行う。 |
| 家族への支援/情報資源 | 以下に関する評価を行う。 ・地域社会あるいはParenttoParentのようなオンラインの情報資源の利用 ・親に対する支援の必要性 |
- 臨床遺伝医、認定遺伝カウンセラー、認定上級遺伝看護師をいう。
予防のための方策
pEDSに伴う歯周組織の破壊は、過炎症反応(hyperinflammatoryreaction)に起因するものである可能性が非常に高い[Gröbnerら2019]。
- 早期にみられる重度歯周炎は、幼児期から厳格な口腔衛生に努めることで軽快する場合がある。
- 3ヵ月に1度、医療者による歯のクリーニングを受けること、ならびに、生涯にわたって自らの手で良好な口腔衛生を保てるよう、高頻度に口腔衛生指導を受けることが不可欠と思われる。
- 歯肉が弱いため、柔らかい歯ブラシが推奨される。
症候に対する治療
治療は、現状の臨床症候に基づき、個別に行われる。
重度の歯周炎が早期から現れるという特徴がみられるため、罹患者は全例、幼児期以降、定期的に歯周病専門医によるチェックを受ける必要がある。現に存在する歯周炎の治療という点では、口腔衛生を良好に保つことが1つの大きな要素である。例を挙げると、歯間部のクリーニングを行う道具や(電動)歯ブラシの使い方を含め、自らの手で良好な口腔衛生を達成するための指導が必須である(「定期的追跡評価」の項を参照)。
一般に、欠損歯の補綴にはデンタルインプラントが用いられることが多いが、pEDSについては、インプラント周囲炎のリスクが高く、インプラントが失敗に終わる可能性が高い[Rinnerら2018]。インプラント周囲炎を起こしたデンタルインプラントは、臨床でよくみられる歯周炎の表現型と全く同じような形で、インプラント周囲の骨に炎症性、進行性の吸収が現れる。
こうしたことから、自分の歯を可能な限り長くもたせるための支援を罹患者に対して行うことこそが、pEDSの口腔に関する治療の第一目標である[Kapferer-Seebacherら2021]。
表5:歯周型Ehlers-Danlos症候群罹患者の症候に対する治療
| 症候/懸念事項 | 治療 | 考慮事項/その他 |
|---|---|---|
| 早期発症型の重度歯周炎 | 歯周治療 | |
| 歯肉退縮 | 特に治療法なし |
|
| 痣のできやすさ/瘢痕化 |
|
|
| 関節可動性亢進 | 理学療法,作業療法,疼痛管理,適切な運動等の必要性に関する助言を目的とした、リウマチ科指導医による評価 | 関節可動性亢進を有する例には、まず一般的助言を行い、その後、必要に応じ適度の運動と理学療法が行われる場合あり。 |
| 動脈瘤/動脈解離 | 部位と状況次第で外科的介入が可能あるいは必要になる場合もあれば、保存的治療(すなわち、反復的画像診断,降圧薬,運動に関する助言)が可能な場合もある。 | |
| 消化器の破裂 | 外科的介入 | |
| 嗄声 | 介入の仕方は、大元の原因により変わってくる。 | 声帯狭窄に対する外科的介入の報告がみられる。 |
定期的追跡評価
表6:歯周型Ehlers-Danlos症候群罹患者で推奨される定期的追跡評価
| 系/懸念事項 | 評価 | 実施頻度 |
|---|---|---|
| 早期発症型の重度歯周炎 | 歯周組織の詳しい評価 | 少なくとも年に1度 |
| 歯周組織のパラメーターの再評価、口腔衛生指導(例えば、歯間部清掃器具や電動歯ブラシの使用)、歯肉縁上・縁下の壊死組織除去等の、支持療法としての歯周ケア | 歯周管理の間隔は、罹患者のニーズにもよるが、おおむね3-6ヵ月が適切である。 | |
| (亜)脱臼や関節痛を伴う関節可動性亢進 | リウマチ科指導医、理学療法士、作業療法士の手で行う。 | 個々の懸念事項により変わってくる。 |
| 動脈瘤/動脈解離のリスク | EDSの治療を行う医療機関の中には、無症状の成人pEDS罹患者に動脈樹の追跡を行い、動脈瘤/動脈解離が認められた例について多職種による治療を行うというところもあるが、pEDSにおける動脈瘤/動脈解離のリスクは不明な部分が多く、血管型EDSより低い模様のため、こうした手法は根拠に乏しい。 | EDSの治療を行う医療機関の中には、無症状の成人pEDS罹患者に対する動脈樹の追跡を1.5-2年に1度の頻度で行うところがある。 |
避けるべき薬剤/環境
pEDS罹患者については、今のところ、特定の活動/治療/薬剤を避けるべきであるとの一般的推奨を裏づけるデータは存在しない。ただ、これは個人個人の状況によって変わってくる要素がある。例えば、動脈瘤を有するpEDS罹患者については、強い衝撃が加わるスポーツや重量挙げのようなものは控えるよう積極的に勧告すべきであろう。
リスクを有する血縁者の評価
予防的歯科衛生や、歯科の通常の治療・定期管理を迅速に開始することで利益が得られる人を可能な限り早期に特定するため、リスクを有するものの見かけ上は無症状の血縁者については、罹患者より年上であるか年下であるかを問わず、その遺伝学的状態を明確にしておくことが望ましい。
リスクを有する血族に対して行う遺伝カウンセリングを目的とした検査関連の事項については、「遺伝カウンセリング」の項を参照されたい。
研究段階の治療
さまざまな疾患・状況に対して進行中の臨床試験に関する情報については、アメリカの「ClinicalTrials.gov」、ならびにヨーロッパの「EUClinicalTrialsRegister」を参照されたい。
注:現時点で本疾患に関する臨床試験が行われているとは限らない。
遺伝カウンセリング
「遺伝カウンセリングは個人や家族に対して遺伝性疾患の本質,遺伝,健康上の影響などの情報を提供し,彼らが医療上あるいは個人的な決断を下すのを援助するプロセスである.以下の項目では遺伝的なリスク評価や家族の遺伝学的状況を明らかにするための家族歴の評価,遺伝学的検査について論じる.この項は個々の当事者が直面しうる個人的あるいは文化的、倫理的な問題に言及しようと意図するものではないし,遺伝専門家へのコンサルトの代用となるものでもない.」
遺伝形式
歯周型Ehlers-Danlos症候群(pEDS)は、常染色体顕性の遺伝形式をとる。
家族構成員のリスク
発端者の両親
- 現在までに報告されている発端者の大多数は、C1RあるいはC1Sの病的バリアントをヘテロで有する罹患者の片親からこれを継承したことでpEDSが生じた例である。
- pEDS罹患者の中には、C1RあるいはC1Sに生じたdenovoの病的バリアントの結果として本疾患に至った例もみられる。ただ、denovoの形で発生したpEDSの占める相対的比率については、よくわかっていない。
- 発端者が家系内で唯一の罹患例(すなわち、孤発例)と目される場合には、発端者の両親に対して分子遺伝学的検査を行って、その遺伝学的状態を明らかにするとともに、再発リスクに関するカウンセリングの信頼性を担保することが推奨される。
- 発端者で同定された病的バリアントが両親いずれからも検出されない場合は、次のような可能性を検討する必要がある。
- 発端者にdenovoの形で病的バリアントが生じた可能性。
- 生殖細胞系列モザイク(もしくは、体細胞・生殖細胞系列両方のモザイク)の片親から、発端者が病的バリアントを継承した可能性。
- pEDSと診断された例の中には、血族の有する疾患を見逃してしまった、症候が明らかになる前の段階で親が死亡してしまった、罹患者である親の発症時期が遅かったといった理由で、いかにも家族歴が陰性であるかのように見えるものもある。こうしたことから、見かけ上、家族歴が陰性であるように思われても、分子遺伝学的検査で、両親とも、発端者で同定された病的バリアントのヘテロ接合者ではないということが証明されない限り、家族歴陰性の確定はできない。
注:(1)発端者で同定された病的バリアントが両親いずれのDNAからも検出されない
(2)親子鑑定により、真正の生物学的父・母であることが確認されている
という2つの条件を満たす場合に、「denovo」という報告がなされる。
親子鑑定がなされていない場合、そのバリアントは「denovo(仮)」と報告されることになる[Richardsら2015]。
注:親の白血球DNAを検査しても、体細胞モザイクの全例を検出できるわけではない。
また、生殖細胞のみに存在する病的バリアントについては、一切検出されない。
C1RあるいはC1Sの病的バリアントを体細胞と生殖細胞系列のモザイクで有する片親の罹患の程度は、理論上、軽度ないしごく軽微であろうと考えられる。
発端者の同胞
発端者の同胞の有するリスクは、発端者の両親の臨床的・遺伝学的状態によって変わってくる。
- 発端者の片親も罹患者であった、ないし、発端者で同定されている病的バリアントを片親も有していたということであれば、発端者の同胞がその病的バリアントを継承するリスクは50%である。pEDS関連病的バリアントを継承する同胞は、個々のヘテロ接合者ごとに症候発現年齢にはばらつきはあるとしても、全員がpEDSの症候を示すようになると考えられる(「浸透率」の項を参照)。
- 発端者の有するpEDS関連病的バリアントが両親いずれの白血球DNAからも検出されないといった場合であれば、発端者の同胞の有するリスクは1%と推定される。それは、理論上、片親が生殖細胞系列モザイクである可能性が残るからである[Rahbariら2016]。
- 両親ともC1RやC1Sの病的バリアントに関する検査を受けていないものの、臨床的には両者とも非罹患者と思われるといった場合であれば、発端者の同胞の有するリスクは低いものと思われる。それでも、臨床的に非罹患者と思われる両親をもつ発端者の同胞は、やはりpEDSのリスクに関してやや高くなるものと考えられる。それは、ヘテロ接合者である片親を正しく診断できなかった可能性、あるいは、理論上、片親が生殖細胞系列モザイクである可能性が残るからである。
発端者の子
pEDS罹患者の子は、50%の確率で、C1RあるいはC1Sの病的バリアントを継承してpEDSの罹患者となる。
他の家族構成員
他の血縁者の有するリスクは、発端者の両親の状態によって変わってくる。仮に、片親がC1RあるいはC1Sの病的バリアントを有していたということになれば、その片親の血縁者にあたる人はすべてリスクを有することになる。
関連する遺伝カウンセリング上の諸事項
早期診断・早期治療を目的としてリスクを有する血縁者に対して行う評価関連の情報については、「臨床的マネジメント」の「リスクを有する血縁者の評価」の項を参照されたい。
家族計画
- 遺伝的リスクの確定、出生前/着床前遺伝学的検査を受けるかどうかの話し合いに最も適しているのは、妊娠前の時期である。
- 罹患者である若い成人、あるいはリスクを有する若い成人に対しては、遺伝カウンセリング(子に生じる可能性のあるリスクや、子をもうける上での選択肢についての説明を含む)を提供することが望ましい。
出生前診断ならびに着床前遺伝学的検査
家系内に存在するpEDSを引き起こす病的バリアントが同定されている場合は、出生前検査ならびに着床前遺伝学的検査を行うことが技術的には可能である。
出生前検査の利用に関しては、医療者間でも、また家族内でも、さまざまな見方がある。現在、多くの医療機関では、出生前検査を個人の決断に委ねられるべきものと考えているようであるが、こうした問題に関しては、もう少し議論を深める必要があろう。
関連情報
GeneReviewsスタッフは、この疾患を持つ患者および家族に役立つ以下の疾患特異的な支援団体/上部支援団体/登録を選択した。GeneReviewsは、他の組織によって提供される情報には責任をもたない。選択基準における情報については、ここをクリック。
- Ehlers-DanlosSocietyHeadquarters
P.O.Box87463
MontgomeryVillageMD20886
Phone:410-670-7577
Email:info@ehlers-danlos.com
www.ehlers-danlos.com
- Ehlers-DanlosSupportGroup
POBox337
AldershotSurreyGU126WZ
UnitedKingdom
Phone:01252690940
Email:director@ehlers-danlos.org
www.ehlers-danlos.org
- Ehlers-DanlosSupportUK
POBox748
BorehamwoodWD69HU
UnitedKingdom
Phone:02087365604;08009078518
www.ehlers-danlos.org
- MedlinePlus
- AssociationFrancaisedesSyndromesd'EhlersDanlos(AFSED)
67,rueJulesLecesne
LeHavre76600
France
Phone:0820203733
Email:contact@afsed.com
- DeutscheEhlers-DanlosInitiativee.V.
Postfach1619
Germany
Email:Info@ehlers-danlos-initiative.de
www.ehlers-danlos-initiative.de
- Ehlers-DanlosSocietyEDS&RelatedDisordersGlobalRegistry
分子遺伝学
分子遺伝学とOMIMの表の情報はGeneReviewsの他の場所の情報とは異なるかもしれない。表は、より最新の情報を含むことがある。
表A:歯周型Ehlers-Danlos症候群:遺伝子とデータベース
| 遺伝子 | 染色体上の座位 | タンパク質 | Locus-Specificデータベース | HGMD | ClinVar |
|---|---|---|---|---|---|
| C1R | 12p13.31 | 補体C1rサブコンポーネント | C1R database | C1R | C1R |
| C1S | 12p13.31 | 補体C1sサブコンポーネント | C1S database C1Sbase: Mutation registry for C1s deficiency |
C1S | C1S |
データは、以下の標準資料から作成したものである。
遺伝子についてはHGNCから、染色体上の座位についてはOMIMから、タンパク質についてはUniProtから。
リンクが張られているデータベース(Locus-Specific,HGMD,ClinVar)の説明についてはこちらをクリック。
表B:歯周型Ehlers-Danlos症候群関連のOMIMエントリー(内容の閲覧はOMIMへ)
| 120580 | COMPLEMENT COMPONENT 1, s SUBCOMPONENT; C1S |
| 130080 | EHLERS-DANLOS SYNDROME, PERIODONTAL TYPE, 1; EDSPD1 |
| 613785 | COMPLEMENT COMPONENT 1, r SUBCOMPONENT; C1R |
| 617174 | EHLERS-DANLOS SYNDROME, PERIODONTAL TYPE, 2; EDSPD2 |
分子レベルの病原
歯周型Ehlers-Danlos症候群(pEDS)は、C1R、C1Sの特定のヘテロ接合性病的バリアントに起因して生じる疾患である。
pEDSの病原に関して中心的役割を果たしているのは、細胞内におけるC1r、C1sの一方あるいは両方の活性化、ならびに、細胞外における活性化型C1sの存在(これにより引き金としての微生物の介在がなくても、古典経路の補体活性化カスケードが活性化される)である。このメカニズムの引き金となるのは、特定の機能獲得型バリアントである[Ballyら2019,Gröbnerら2019]。
疾患の発症メカニズム
これらのバリアントの病原メカニズムは、これらの遺伝子のホモ接合性の機能喪失や、C1エステラーゼインヒビターの欠損とは全く別物である。トランスフェクションを行ったヒト胎児腎細胞293(HEK細胞)、ならびに罹患者から採取した線維芽細胞の機能研究により、pEDSを生じさせる16種のバリアントすべてにおいて、正常なC1複合体を形成するための結合が障害され、細胞外C1r/C1sセリンプロテアーゼの異常な活性化が生じることが明らかとなった。pEDSの病原としてのC1Rのバリアントは、C1r断片の細胞内残存、凝集体の分泌、C1rの新たな切断部位の形成といった、細胞内プロセシングや分泌に、独特でドメイン特異的な異常を示した。1つのバリアントは、C1qの結合部位を無能化するものであった。罹患者から採取して利用できたすべての線維芽細胞は、C4を活性化することなく酵素前駆体C1sを分泌するコントロールの細胞株とは対照的に、上清内のC1sの活性化と外部から加えたC4の活性化を示した[Gröbnerら2019]。同様に、C1S関連pEDSの機能研究では、その研究を行った時点で知られていたC1Sの2種の病的バリアントのどちらにおいても、C1sタンパク質のCCP1ドメインの末端部で、トリプシン様、あるいはC1s様の切断が生じていることが明らかになっている[Ballyら2019]。
C1rやC1sのセリンプロテアーゼとしての機能を奪うようなバリアント、例えば大規模なゲノム再配列、アウトオブフレームの欠失や重複、ナンセンスバリアントなどについては、pEDSの原因になることはないと考えられている。ただ、インフレームの欠失や重複については、pEDSの原因になる可能性を完全に否定することまではできない現状である。
遺伝子特異的な検査技術上の考慮事項
pEDSを引き起こすバリアントの範囲は、C1SよりC1Rのほうが広い。これは、C1エステラーゼインヒビター非存在下で、在来のC1rが自己触媒活性を有することに起因するものであるように思われる。C1Rのバリアントが自己活性化の阻害を妨げる場合にpEDSとなって現れるのに対して、C1Sのバリアントのほうは、自己活性化の引き金となる場合にのみpEDSを引き起こすようである。こうしたことは、この両遺伝子に生じた意義不明バリアントの解釈にも関係してくることである。上記のことは、C1RやC1SのヌルバリアントによってpEDSが生じない理由を説明するものともなっている。
更新履歴:
-
Gene Reviews著者: Ines Kapferer-Seebacher, DMD, Fleur S van Dijk, MD, PhD, and Johannes Zschocke, MD, PhD.
日本語訳者: 佐藤康守(たい矯正歯科)、櫻井晃洋(札幌医科大学医学部遺伝医学)
GeneReviews最終更新日: 2021.7.29. 日本語訳最終更新日: 2023.4.7.[in present]