PTEN過誤腫症候群
(PTEN Hamartoma Tumor Syndrome)
[Synonyms:PTHS]
GeneReviews著者: Lamis Yehia, PhD and Charis Eng, MD, PhD.
日本語訳者:箕浦祐子(札幌医科大学大学院医学研究科遺伝医学)櫻井晃洋(札幌医科大学附属病院遺伝子診療科 )
GeneReviews最終更新日: 2021.2.11 日本語訳最終更新日: 2021.3.1
原文 PTEN Hamartoma Tumor Syndrome
要約
疾患の特徴
PTEN過誤腫症候群(PHTS)には、Cowden症候群(CS)、Bannayan-Riley-Ruvalcab症候群 (BRRS)、PTEN関連Proteus症候群 (PS)および Proteus様症候群が含まれる。
- CSは多発性過誤腫症候群であり、甲状腺、乳房、腎臓、子宮内膜に良性ないし悪性の腫瘍を生じるリスクが高い。患者は通常、巨頭症、外毛根鞘腫、乳頭腫性丘疹を有し、これらは20歳代後半までに発症する。乳がんを発症する生涯リスクは85%で、診断年齢の平均は38~46歳である。甲状腺がん(通常は濾胞がんだが、稀に乳頭がんがある。しかし髄様がんはない)の生涯リスクは約35%である。腎細胞がん(組織型は乳頭状が主体)の生涯リスクは34%で、子宮内膜がんのリスクは約28%である。
- BRRSは巨頭症、 過誤腫性 消化管ポリポーシス、 脂肪腫および陰茎亀頭の色素斑を特徴とする先天性疾患である。
- PS は結合組織母斑、表皮母斑、骨化過剰症のみならず、先天性奇形や複数組織の過誤腫性異常増殖など複雑で臨床像が多彩な疾患である。
- Proteus様症候群は定義づけられていないが、PSの診断基準は満たさないものの、PSの臨床的特徴を顕著に示す患者に対して用いられる。
診断・検査
PHTSの診断は、発端者において分子遺伝学検査によるヘテロ接合型の生殖細胞系列PTEN 病的バリアントの同定によって確立される。
臨床的マネジメント
病変の治療:
PHTSの良性病変および悪性病変の治療は、散発性の場合と同様である。CSの皮膚粘膜症状は局所薬(例えば5-フルオロウラシル)、掻爬術、凍結外科手術またはレーザー切断によって緩和されるかもしれないが、実施されることは 稀である。皮膚病変は悪性が疑われるか、症状( 痛み、変形、瘢痕化の増加など)が顕著である場合に限って切除されるべきである。
検診:
腫瘍を最も治療しやすい段階で、最も早期に発見するために下記が推奨される。
- 小児(18歳未満):診断時(最年少の報告は7歳)から年一回の甲状腺超音波検査と身体検査時の皮膚のチェック
- 成人:年一回の甲状腺超音波検査と皮膚科検査
- 女性30歳以降:毎月の乳房の自己検診、年一回の乳房スクリーニング(少なくともマンモグラム、MRIも組み合わせると良い) 。35歳以降は、経膣超音波検査または子宮内膜の生検も考慮する。
- 男性と女性:35歳から大腸内視鏡検査を開始し、頻度は同定されたポリポーシスの程度あるいは若年発症(40歳未満)の大腸がん家族歴に応じ る。40歳 から2年に一度の腎臓の画像解析(CTかMRIが望ましい)を始める。
- 若年齢で特定のタイプのがんの家族歴を有する被験者:家系内で診断を受けた最も若い年齢から5-10歳若い年齢でスクリーニングの受診を始める。
リスクのある 血縁者の検査:
発端者にPTEN 病的バリアント が同定された場合、症状はないがリスクのある 血縁者の分子遺伝学的検査を実施することにより、その家系特異的 病的バリアントをもつ 血縁者を同定し、検診を実施する正当な理由を得ることができる。
遺伝カウンセリング
PHTSは常染色体優性遺伝形式で遺伝する。CSは診断率が低い傾向があるため、孤発性(明らかな家族歴がない患者と定義される)および家族性(家系に2名以上の患者がいると定義される)の実際の割合はわからない。CS症例は大多数が孤発性である。CS患者のおそらく10~50%に罹患した親がいる。患者の子にはそれぞれ50%の確率で 病的バリアントが遺伝し、PHTSを発症する。家系内でPTEN 病的バリアントが同定されている場合、リスクが高い妊娠に対する出生前診断が可能である。
訳注:日本では,本症に対する出生前診断は行われない.いずれにしても次世代への遺伝に関しては細心の遺伝カウンセリングが必要である.
GeneReviewの 記載範囲
| PTEN過誤腫症候群:含まれる表現型1 |
|---|
|
同義語と旧式の名称は 命名規則を参照 すること。
- これらの表現型の他の遺伝的要因については,鑑別診断を参照のこと.
診断
PHTSが疑われる所見
PTEN 過誤腫症候群(PHTS) にはCowden症候群(CS)、Bannayan-Riley-Ruvalcab症候群 (BRRS)、PTEN関連Proteus症候群 (PS)およびProteus様症候群が含まれる。
以下の臨床的特徴を呈する患者では、PTEN 過誤腫症候群(PHTS) を疑うべきである。
Cowden症候群(CS). 3,000例を超えるCSまたはCowden様症候群(C LS)の患者の前向き研究で集められたデータに基づき、表現型と診断時の年齢を考慮に入れた採点システム(オンラインで閲覧可能)が開発された。この採点システムにはCS/ CLSが疑われる患者の臨床情報の入力が可能で、その結果、PTEN 病的バリアントを検出する事前 確率が算出される。
- 成人では、臨床閾値スコア≥10でPHTSを考慮して遺伝学の専門家に紹介することが推奨される。
- 小児では、巨頭症および下記項目 が 1つ以上 あれば、PHTSが考慮される。
- 自閉症又は発達遅延
- 脂肪腫、外毛根鞘腫、口腔乳頭腫または陰茎の色素斑を含む皮膚の特徴
- 動静脈奇形または血管腫といった血管の特徴
- 消化管のポリープ
- 小児期発症の甲状腺がんまたは胚細胞腫瘍
さらに、CS のコンセンサス臨床診断基準が作成され[Eng 2000]、National Comprehensive Cancer Network (訳注:全文の閲覧には登録が必要)により 毎年更新されている。しかし、このセクションで解説されているCS採点システムは、NCCN診断基準より正確であることが示されている[Tanら 2011]。
NCCNのコンセンサス臨床診断基準は、特徴的 基準、大基準、小基準の3群に分類される。
臨床診断基準
- 成人型Lhermitte-Duclos病(LDD)、小脳異形成神経節細胞腫の存在で定義される[Zhouら 2003a]
- 粘膜皮膚病変
- 外毛根鞘腫(顔面)(図1参照)
- 肢端角化症
- 乳頭腫様病変(図2参照)
- 粘膜病変
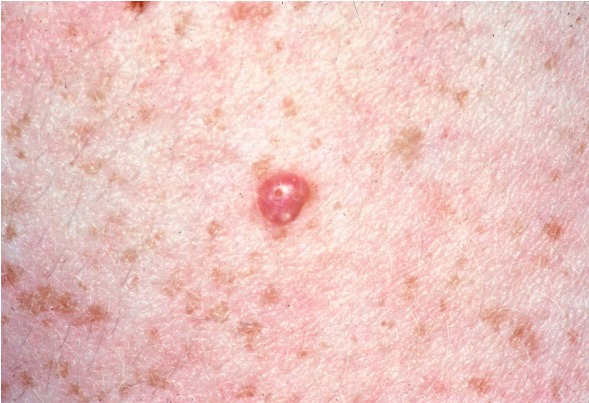 |
図 1.外毛根鞘腫 |
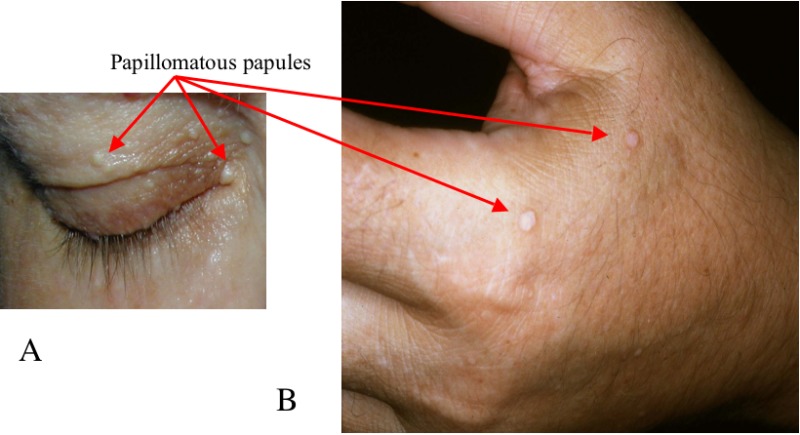 |
図 2. 眼の周辺(A)と手の甲(B)の 乳頭腫の丘疹 |
大基準
- 乳がん
- 上皮性甲状腺 がん(髄様がん以外)、特に甲状腺濾胞がん
- 巨頭症 (前後頭囲≥97パーセンタイル)
- 子宮内膜 がん
小基準
- その他の甲状腺病変(例、腺腫、多結節性甲状腺腫)
- 知的障害(IQ ≦ 75)
- 過誤腫性消化管ポリープ
- 乳房の線維嚢胞性疾患
- 脂肪腫
- 線維腫
- 泌尿生殖器系腫瘍(特に腎細胞 がん)
- 泌尿生殖器奇形
- 子宮筋腫
CSの 臨床的診断は、下記基準の内いずれか一つを満たす場合に 確定する:
- 下記の内のいずれかを含む特徴的な皮膚粘膜病変 :
- 6つ以上の顔面丘疹で、その内の3つ以上は外毛根鞘腫
- 顔面 皮膚 丘疹および口腔粘膜 乳頭腫症
- 口腔粘膜 乳頭腫症および肢端角化症
- 6 ヶ所以上の掌蹠角化症
- 2つ以上の大基準
- 大基準1つと3つ以上の小基準
- 4つ以上の小基準
上記のCSの診断基準に適合する者が家族にいる場合は、血縁者が下記基準の内いずれか一つを満たす場合に CSの臨床的診断とみなす。
- 特徴的基準
- 小基準の有無にかかわらず1つ以上の大基準
- 2つの小基準
- Bannayan-Riley-Ruvalcab症候群の病歴
Bannayan-Riley-Ruvalcab症候群 (BRRS). BRRSの診断基準は決まっていないが、大きくは、巨頭症、過誤腫性消化管ポリポーシス、脂肪腫、陰茎亀頭の色素斑の主 な特徴に基づいて診断される[Gorlinら 1992]。
PTEN関連Proteus症候群(PS)は非常に多様であり、 典型的には生殖細胞系列のヘテロ接合性PTEN病的バリアントと、罹患臓器にモザイク状に分布する潜在的で後天的な体細胞PTEN病的バリアントを特徴とする[Zhouら 2000]。そのため、共通の診断基準が作成されているにもかかわらず、しばしば誤って診断されることがある[Bieseckerら 1999] ( Proteus症候群を参照のこと)。これがPTENの専門家たちがPHTSの分子的な診断を推奨する理由である。
PTEN関連Proteus様症候群の定義は決まっていないが、診断基準を満たさず、生殖細胞系列のヘテロ接合性PTEN病的バリアントを有する、PSの臨床的特徴を顕著に示す 患者と説明される。注:臨床的属性はなくても、PHTSの分子的な診断を用いることが最も正確と考えられる。
診断の確定
PHTSの診断は、発端者において分子遺伝学検査によるヘテロ接合型の生殖細胞PTEN 病的バリアントの同定によって確立される(表1を参照)。
分子遺伝学検査の手法には、表現型に応じて、遺伝子標的検査(単一遺伝子検査、マルチジーンパネル) や 包括的 ゲノム検査(エクソームシークエンス、ゲノムシークエンス解析)の組み合わせが ある。
遺伝子標的検査を行う場合は、臨床医がどの遺伝子に関連がありそうか決める必要があるが、ゲノム検査の場合はその必要はない。“疑わしい所見”に記載のあるような特徴的な所見があれば、遺伝子標的検査で診断がつくかもしれないが(Option 1参照)、巨頭症や発達遅延、若年発症腫瘍など他の多くの遺伝性疾患と見分けのつかない表現型の場合は、ゲノム検査を利用した方が診断がつきやすいだろう(Option 2参照)。
Option 1
単一遺伝子検査:最初にPTENの配列解析が行われ、 病的バリアントが発見されなければ遺伝子を標的とした欠失 /重複解析が行われる。欠失 /重複解析によっても 病的バリアントが発見されなければ、PTENの遺伝子発現 を低下 させる バリアント について、PTENプロモーター領域の配列解析 を行う。
注:Cowden症候群(CS)とCowden様症候群(CLS)の患者においては、生殖細胞系列KLLN のエピ変異、PIK3CA、 AKT1 [Orloffら 2013] SEC23B [Yehiaら 2015]、およびWWP1 [Lee ら 2020]を含むSDHB-D 解析 も考慮される(鑑別診断、PHTSでないCS患者とCLS患者における検討を参照)。
PTEN と他の関連する遺伝子(鑑別診断を参照)を含むマルチジーンパネルも考慮される 。注 :(1)パネルに含まれる遺伝子と各遺伝子に用いられる試験の診断感度は検査施設と時期によって異なる。(2) マルチジーンパネルには、このGeneReviewでは言及されていない症状に関連する遺伝子が含まれることが有る。従って、医師は、意義不明なバリアントや根本的な表現型を説明できない遺伝子の病的バリアントの検出を避けながら、症状の遺伝的原因を同定するために最適な機会を最も適正な価格で提供し得る マルチジーンパネルを決定する必要がある。(3) 検査施設によっては、臨床医が指定した遺伝子を含む、カスタム設計された施設独自のパネルや、表現型に焦点を当てたエクソーム解析パネルといった選択肢もある。(4)パネルで用いられる方法には、配列解析、欠失 /重複解析、他の配列に拠らない手法のすべてまたはいずれかが含まれる。
マルチジーンパネルに関する概要はここをクリック。遺伝学的検査を発注する臨床医向けのより詳細な情報についてはこちらを参照のこと。
Option 2
包括的なゲノム検査では、医師が関連のありそうな遺伝子を決める必要はない。エクソームシークエンス解析が一般的に用いられるが、ゲノムシークエンス解析も可能である。
包括的なゲノム検査に関する概要はここをクリック。ゲノム検査を発注する臨床医向けのより詳細な情報についてはこちらを参照のこと。
表1. PTEN過誤腫症候群に用いられる分子遺伝学検査
| 遺伝子1 | 検査法 | 各方法で検出される 病的バリアント2の表現型を有する発端者の割合 | |||
|---|---|---|---|---|---|
| CS | BRRS | PLS | PS | ||
| PTEN | コーディング領域の配列解析3 | 25%-80% | 60% | 50%4 | 20%4 |
| 欠失/重複解析 5 | 3% 6 | 11%7 | 不明 | 不明 | |
| プロモーター領域の配列解析 3 | 10%7 | まれ7 | 不明 | 不明 | |
BRRS = Bannayan-Riley-Ruvalcab症候群;CS = Cowden症候群;PLS = Proteus様症候群;PS = PTEN関連Proteus症候群
- 染色体 座位とタンパク質については 表A. 遺伝子とデータベース を参照のこと。
- この遺伝子で検出されるバリアント情報については、分子遺伝学の項を参照。
- 配列解析では良性、おそらく良性、臨床的意義は不明、おそらく病 的、あるいは病 的の バリアントが検出される。 病的バリアントには小さな遺伝子内欠失/挿入、ミスセンス、ナンセンス、スプサイス部位 バリアントが含まれる。通常は エクソンまたは遺伝子全体の欠失 /重複は検出されない。配列解析結果の解釈に関して考慮すべき問題についてはこちらを参照のこと。
- Proteus様症候群の患者の50%以下、Proteus症候群の臨床診断基準に適合する患者の20%以下 では、PTEN 病的バリアントを有することがデータによって示唆されている [Yehia & Eng 2018, Yehia ら 2019]。
- 遺伝子標的欠失/重複解析は、遺伝子内の欠失や重複を検出する。定量的PCR、広域PCR、多重ライゲーション依存プローブ増幅(MLPA)や、単一エクソンの欠失や重複を検出するために設計された遺伝子標的マイクロアレイ などの多様な手法が用いられる。
- 広範囲の欠失のあるCS患者についての報告がある[Tan ら 2011, Yehia ら 2019]
- [Zhouら 2003b].。
臨床的特徴
臨床像
PTEN過誤腫症候群(PHTS)は、過誤腫と生殖細胞系列PTEN 病的バリアントを特徴とする。臨床的に、PHTSにはCowden症候群(CS)、Bannayan-Riley-Ruvalcaba症候群(BRRS)、PTEN関連Proteus症候群(PS)およびPTEN関連Proteus様症候群が含まれる。
- CSは甲状腺、乳房、子宮内膜の良性腫瘍および悪性腫瘍のリスクが高い多発性過誤腫症候群である。 腎細胞がんと大腸がんもPHTSに含まれる。
- BRRSは巨頭症、消化管ポリポーシス、脂肪腫、血管の奇形、陰茎亀頭の色素斑を特徴とする先天性疾患である。
- PSは先天性奇形と複数組織の過剰増殖を含む、複雑で非常に多様な疾患である。
- Proteus様症候群は定義されていないが、PSの診断基準は満たさないものの、PSの臨床的特徴を顕著に示す患者に対して用いられる。
Cowden症候群(CS). 90%を超えるCS患者では、20代後半までに何らかの臨床所見が認められる[Nelenら 1996, Eng 2000]。30歳までに患者の99%は、 肢端角化症と足底角化症、粘膜皮膚徴候(主に外毛根鞘腫と乳頭腫様丘疹)を発症する。さらにCowden症候群の患者は通常、巨頭症と長頭症を呈する。
過誤腫性および混在型消化管ポリープはPHTS患者の大半でしばしば認められるが、これは大腸がんのリスクを高めることに寄与する[Healdら 2010]。
事例観察によれば、CSの特徴が存在する場合にグリコーゲンを含む扁平上皮の過形成(glycogenic acanthosis)が認められると、高い確率でPTEN 病的バリアントが発見されるようである[ McGarrityら 2003]。
腫瘍のリスク. CS患者は乳がん、甲状腺がん、腎がん、子宮内膜 がんのリスクが高い。他の遺伝性がん症候群と同様に、多発性および両側性(乳房などの対になった臓器)がんのリスクが上昇する。生殖細胞系列のPTEN病的バリアントがあると、2つ目の原発性悪性新生物ができるリスクが、一般集団より7倍高くなる[Ngeow ら 2014]。
- 乳房の疾患
- Cowden症候群の女性は、良性の乳房疾患が67%と高いリスクを有する。
- PTEN 病的バリアントを有する 発端者とその家族の前向き研究で集められ追跡されたデータの解析によると、女性における乳がんの生涯リスクは85%で、50歳までの浸透 率は50%であった[Tanら 2012]。
- PTEN 病的バリアントを有する男性における乳がんも報告されているが[Fackenthalら 2001]、3000例を超える発端者を含む研究では観察されていない[Tanら 2011]。
- 甲状腺の疾患
- 腺腫性甲状腺腫と濾胞性腺腫のみならず、良性の多結節性甲状腺腫が多く認められ、CS患者の最大で75%に発症する[Harachら 1999]。
- 上皮性甲状腺 がんの 生涯リスクは約35%である[Tanら 2012]。発症の年齢中央 値は37歳であり、診断時の最少年齢は7歳であった[Ngeowら 2011]。
注 :(1)一般の集団では乳頭 腫の組織学所見が多く認められるが、成人では濾胞性腫の組織学所見が多く観察される。(2)分子学的にCSが確認されたコホートでは甲状腺髄様がんは観察されていない。
- 子宮内膜の疾患
- 良性の子宮筋腫が多く認められる。
- 子宮内膜がんの生涯リスクは28%と推定され、リスク が上がり始めるのは30代後半から40代 前半である[Tanら 2012]。
- 消化管の新生物
- 上部または下部消化管の内視鏡検査を少なくとも一度受けた PTEN 病的バリアント 保有者の90%以上 で ポリープが発見された[Healdら 2010]。組織学所見は、神経節 細胞腫性ポリープから過誤腫性ポリープ、若年性ポリープまたは腺腫性ポリープと様々であった。
- 大腸がんの生涯リスクは9%と推定され、リスクが上がり始めるの は30代後半である[Tanら 2012]。
- 腎細胞がん(RCC).
- RCCの生涯リスクは35%と推定され、リスクが上がり始めるの は20 代である[Tanら 2012, Kim ら 2020]。主な組織学所見は乳頭状腎細胞がんである[Mesterら 2012]。
- 皮膚悪性黒色腫.皮膚悪性黒色腫の生涯リスクは6%と推定され、最も早い発症は3歳である[Tanら 2012]。
- その他
- 脳腫瘍および何らかの臓器を冒す血管奇形はCS患者に時折認められる。
- 稀な中枢神経系の腫瘍である小脳異形成神経節細胞腫(Lhermitte-Duclos病)もCSに認められ、これはおそらく特徴的な症状であると考えられる。
注 : 髄膜腫は一般集団においても多くみられるため、髄膜腫 が実際にCSの 症状であるかは不明である。
Bannayan-Riley-Ruvalcab症候群 (BRRS). BRRSの一般的な特徴には上記に加えて、高出生体重、発達遅延、 知的障害(患者の50%)、近位筋における筋障害 (60%)、関節の過伸展、漏斗胸、脊柱側弯症(50%)が含まれる[Gorlin ら 1992] 。
PTEN 病的バリアントを有するBRRS患者はCS患者と 同様のがんリスクを有すると考えられているが、正式な研究は行われていない。注 :これらのリスクがPTEN 病的バリアントをもたないBRRS患者にも当てはまるか否かは明らかでない。
BRRSにおける過誤腫性消化管ポリープ(患者の45%に見られる)は時に腸重積 を伴うが、直腸の出血および「血清」の滲出がより一般的に認められる。このポリープは大腸がんのリスクを上昇させるとは考えられていない。PHTS過誤腫性ポリープはPeutz-Jeghers症候群で認められるポリープとは組織形態学的に異なる。
PTEN関連Proteus症候群 (PS) は全ての胚葉に由来する多様な組織における進行性の分節的あるいはパッチ状の過剰増殖を特徴とし、骨格、皮膚、脂肪および中枢神経系を冒すことが最も多い。Proteus症候群の患者のほとんどは出生時には 症状は無いかあるいは最小限であり、幼児期に発症して急激に進行し、小児期を通して絶え間なく進行して、重篤な過度の発育と外観の変形を引き起こす。これには広範な腫瘍と肺の合併症を伴い、深部静脈血栓症と肺塞栓症の顕著な素因ともなる。詳細はProteus症候群を参照のこと。
PTEN関連Proteus様症候群は定義づけられていないが、PSの診断基準は満たさないがPSの臨床的特徴を顕著に示す患者に対して用いられる。
すべてのPHTS表現型の臨床的意義
生殖細胞系列PTEN病的バリアントを有する患者の2つの最も重大な臨床的特徴は、臓器特異的ながんと自閉症スペクトラム障害(ASD)を含む神経発達障害である。
PTENに関連する腫瘍形成の生涯リスク.臨床的診断に関わらず、生殖細胞系列PTEN病的バリアントを有する者では、CS患者と同様のがんのリスクを持つと考えられる[Tan ら 2012]。
神経発達障害.巨脳症やASD、発達遅延などの神経発達に関する表現型がPHTS患者で報告されている[Goffin ら 2001, Butler ら 2005, Hansen-Kiss ら 2017]。ASDと巨頭症のある患者の10-20%で、生殖細胞系列PTEN病的バリアントが同定されている[Yehia ら 2020]。PTENに関連するASDでみられる巨頭症の程度は、PTENとは無関係の巨頭症ASD患者よりも重度であることが多い[Mester ら 2011]。PTENに関連するASD患者では、大脳皮質における白質細胞の増加および言語発達の遅れ、作業記憶や処理速度の低下、適応性や感覚の異常を含む特異的な神経認知機能や行動の表現型を示す[Frazier ら 2015, Busch ら 2019]。
遺伝型と臨床型の関連
PTEN の遺伝型と表現型の解析を目的として、血縁関係のないCSの発端者37例がInternational Cowden Consortiumで提唱された 運用上の診断基準 1995年版を用いて確認された[Nelenら 1996, Eng 2000]。関連 解析により、生殖細胞 系列PTEN 病的バリアントをもつCS家系では、PTEN 病的バリアントをもたない家系に比べて乳房の悪性疾患を発症する傾向が高いことがわかった[Marshら 1998]。さらに、 病的なミスセンス バリアントや、5’ 末端から ホスファターゼのコア配列まで 、あるいは ホスファターゼのコア配列内の バリアントは、5つ以上の臓器の合併症と関連することがわかっており、これは疾患の重篤度を示す代替表現型(surrogate phenotype)であった[Marshら 1998]。
CSとBRRSを重複して有する家系のうち90%を超える家系で、生殖細胞系列 PTEN 病的バリアントが認められた。BRRSとCSの 変異 スペクトルが重なっていることが示されて いる。BRRSについて、家系内で一人 だけ発症する場合と、複数に発症する場合とで、遺伝子変異の頻度に差はなかった。
片側肥大症、巨頭症、脂肪腫、結合組織母斑、多発性動静脈奇形を示すProteus様症候群の孤発例(明らかな家族歴がないもの)の患者1例において、生殖細胞系列にp.Arg335TerのPTEN 病的バリアントと、3つの異なる組織に同じ体細胞 病的バリアント(p.Arg130Ter)が見つかり、これはおそらく生殖細胞モザイク現象と思われる[Zhouら 2000]。これらの 病的バリアントはいずれも 臨床的にCSとBRRSの特徴をもつ患者においてすでに記述されている。
Proteus症候群の臨床的診断基準を満たす患者9例中2例とProteus様症候群患者の6例中3例で、生殖細胞系列 PTEN 病的バリアントが見つかった。それ以来、Proteus症候群 の臨床的診断基準に適合する患者において、生殖細胞系列 PTEN 病的バリアント が複数報告されている[Yehia & Eng 2018] 。
浸透率
CS患者の90%を超える患者では、20代後半までに疾患の何らかの臨床所見が認められる[Nelen ら 1996, Eng 2000, Yehiaら2020] 。30歳までに患者の99%で、外毛根鞘腫と乳頭腫様丘疹を主とし、 肢端角化症と足底角化症を含む粘膜皮膚徴候が現れる。( Cowden症候群で特定の徴候が顕現化する年齢については臨床記述を参照のこと)
病名
Cowden症候群、Cowden病および多発性過誤腫症候群は同義的に使用されてきている。
Bannayan-Riley-Ruvalcaba症候群、Bannayan-Ruvalcaba-Riley症候群、Bannayan-Zonana症候群およびMyhre-Riley-Smith症候群は、著者らがBRRSと呼ぶ類似した一連の徴候を示すものを称する。PTEN 病的バリアントが検出された場合には、遺伝子に関連した名称であるPHTSが使用されるべきである。
Zhouら[2000] によって最初に発表された臨床症状および生殖細胞系列 PTEN 病的バリアントを示すProteus様症候群の一つの形態は、SOLAMEN (segmental overgrowth分節的過成長, adipomatosis脂肪腫, arteriovenous malformation動静脈奇形 , epidermal nevus表皮母斑)症候群と命名された[Cauxら 2007]。臨床的マネジメントに対して意味するところを鑑みて、PTEN 病的バリアントに関連するいかなる表現型もPHTSと称されるべきであるので、特に分子の時代においては、SOLAMEN症候群は有用な名称ではない[Yehia ら 2020] 。
CSの診断を確立するのは難しいため、実際の有病率は不明である。頻度は20万分の1と推定されているが[Nelenら 1999]、おそらくは過小評価されているだろう。CSおよびBRRSは多様であり、しばしば外的所見は とらえにくいため、患者の多くは診断に至っていない[Yehia ら 2020] 。
遺伝学的に関連する疾患
PTEN 生殖細胞系列病的バリアントに関連する可能性のある表現型を表2.にまとめた。
表2. PTEN関連 疾患
| 疾患 | 臨床的特徴 | 解説 |
|---|---|---|
| 他に明らかな症状のないLhermitte-Duclos 病 (LDD) | 他に明らかな症状のない小脳異形成性神経節細胞腫 | CS/BRRSの臨床的所見がなくても、(すべてではないが)ほとんどの成人発症のLDDは、PTEN 病的バリアントを原因とすると考えらえる。 注: 生殖細胞系列PTEN 病的バリアントは小児期発症のLDD患者ではあまりみられない。1 CS/BRRSの他の症状がないか、LDD以外に明らかな症状のない患者のすべてを評価した。 |
| 自閉症/広汎性発達障害および 巨頭症 (OMIM 605309) | ASD および巨頭症 | ASD および巨頭症患者の10-20%が、生殖細胞系列PTEN 病的バリアントを有する。2 |
| 幼少期の若年性ポリポーシス(JPI; Juvenile polyposis of infancy) (OMIM 612242) |
6歳未満で診断された若年性ポリポーシス; 消化器症状はしばしば重篤である。(出血・下痢・蛋白質漏出性腸症) | BMPR1A およびPTENの生殖細胞系列の欠失により、稀な症状が現れる; JPIの外面的な徴候はBRRSに類似することがある。 |
ASD = 自閉症スペクトラム障害; BRRS = Bannayan-Riley-Ruvalcaba 症候群; CS = Cowden 症候群
- Zhou ら [2003a]
- Butlerら [2005], Hansen-Kiss ら [2017], Yehia ら [2020]
単独の腫瘍として発生し、他のPHTS所見のない散発性腫瘍(子宮内膜がん、前立腺がん、膠芽腫など)では、生殖細胞系列には存在しない PTEN の体細胞性バリアントとしばしば関連する。この状況における腫瘍の疾患素因(易罹患性)は遺伝しない。より詳しい情報は、がんと良性腫瘍の項を参照のこと。
鑑別診断
表 3.PTEN過誤腫症候群の鑑別診断において検討すべき疾患
| 遺伝子(群) | 疾患 | 臨床的特徴 | 解説 |
|---|---|---|---|
| AKT1 | AKT1関連Proteus症候群1,2 | 進行性の分節的あるいはパッチ状の過剰増殖が、主として骨格、皮膚、脂肪および中枢神経系を冒す;広範な腫瘍と肺の合併症を引き起こし、深部静脈血栓症と肺塞栓症の顕著な素因ともなる。 | PHTSは異常増殖と線状母斑および血管奇形と関連する。これらは臨床的・分子学的に、AKT1関連Proteus症候群とはまったく異なる。 |
| BMPR1A SMAD4 |
若年性ポリポーシス(JPS; Juvenile polyposis syndrome) | 消化管に過誤腫性ポリープを形成しやすい(特に、胃・小腸・結腸・直腸)。ポリープの治療をしないと出血や貧血の原因となりうる。ほとんどの若年性ポリープは良性だが、悪性腫瘍への転換も起こりうる。 | PHTSとは異なり、通常20歳までに ポリープ が表れ、 一生のうちに100 個に達する場合もある。 JPSのポリープは組織学的に若年性ポリープである。PHTSのポリープは、組織学的には、上皮性過形成、過誤腫、神経鞘腫、若年性、腺腫など多様である。 |
| FLCN | Birt-Hogg-Dubé 症候群1 | 皮膚所見(線維毛包腫、軟性線維腫、血管線維腫、口腔内丘疹、皮膚 コラゲノーマ、表皮嚢胞)、肺嚢胞/気胸の既往と様々なタイプの腎腫瘍 | 皮膚病変は、 PHTSの特徴である外毛根鞘腫と間違われやすい。 PHTSでよくみられる乳頭状腎がんと異なり、BHDでは嫌色素性/ オンコサイトーマの組織型が混在する。 |
| NF1 | 神経線維腫1型(NF1) 1 | NF1とCS/BRRSに唯一共通する所見は、カフェオレ斑と皮膚の線維腫である。 | CS/BRRS患者に消化管に神経節細胞腫が存在する ことで、NF1と誤って診断されることがある。 |
| PTCH1 SUFU |
基底細胞母斑症候群(NBCCS)1 | 顎に多発する角化嚢胞や基底細胞がん;骨格異常;異所性石灰化;および約60%の患者では、巨頭症や前額部の瘤、粗野な顔貌、顔面の稗粒腫といった外観所見がみられる。 | CSとNBCCS における皮膚所見や発達の特徴は大きく異なる。 |
| STK11 | Peutz-Jeghers症候群 | 消化管ポリポーシス、皮膚粘膜の色素沈着およびがんの易罹患性 | P-Jのポリープは診断がつきやすく、CSやJPSの過誤腫性ポリープとは明らかに異なる。P-Jのポリープはしばしば症状(腸重積や直腸の出血)を伴うが、CSのポリープでは稀である。 |
BRRS = Bannayan-Riley-Ruvalcaba 症候群; CS = Cowden 症候群; PHTS = PTEN 過誤腫症候群; P-J = Peutz-Jeghers
- Birt-Hogg-Dubé症候群、神経線維腫1型、基底細胞母斑(Gorlin)症候群は、常染色体優性形式で遺伝する。
(GeneReviewのProteus症候群の著者らにとって既知の)臨床的に診断が確定されたProteus症候群の患者は全て、特異的なde novo AKT1 病的バリアント c.49G>A (p.Glu17Lys)の体細胞モザイク現象に起因する孤発性の症例である。 - PTENはリン酸化を低減させてAKT1を下方制御するので、Proteus症候群で活性化されたAKT1 病的バリアントが発見されたことは、Proteus症候群が「PTEN経路に関する 疾患」(PTEN-pathway-opathy)であることを確認するものである。
PHTSでないCowden症候群(CS)およびCowden様症候群(CLS)患者で考慮すること
- 生殖細胞KLLNエピ変異.
PTENの生殖細胞系列 病的バリアントを持たない CS (OMIM 615107) と CLSの患者の約30%は、生殖細胞系列KLLNのメチル化 エピ変異を有 し[Yehia & Eng 2020] 、これはPTENではなくKLLMの発現の下方制御を招く。注目されるのは、KLLNはPTENと双方向性プロモーターを共有していることである。 試験的なデータでは、生殖細胞系列KLLNエピ変異を有するCSおよび CLS患者は、生殖細胞系列 PTEN 病的バリアントを有する患者に比べて、乳がんと腎細胞がんの有病率が高いことが示唆された。 注:現在では、KLLNのメチル化は技術的な問題があり、臨床的には用いられていない。
- PHTSでないCSとCLS患者の感受性遺伝子.
ある予備的研究で、生殖細胞 系列PTEN 病的バリアントをもたない(が、マンガンスーパーオキシドジスムターゼMnSODの数値が高い) CS とCSL 患者は、SDHBとSDHD の生殖細胞系列 バリアント と関連することがわかった[>Niら 2008]。PTEN 病的バリアントを持たないCS またはCSLの患者の約10%にSDHB、SDHCとSDHD の生殖細胞系列 バリアントが生じることは、608例の被験者を対象とした独立した研究において妥当性が確認された[Yehia & Eng 2020]。これらの バリアントは、HIF1aの安定化、NQ01相互作用の低下に 伴うp53の二次的不安定化、および活性酸素種の増加と その結果としてのアポトーシス耐性に関与している。PTENまたはSDHx に生殖細胞系列 病的バリアント を持たないCSおよびCSL患者の約10%は、PIK3CA (PIK3CA関連分節的過 形成を参照)またはAKT1に生殖細胞系列 病的バリアントを有するrloffら 2013]。上記の既知遺伝子に 病的バリアントを持たない別のCSおよびCSL患者の3 -6%は、特に甲状腺 がんとリボソームの発生強化に 関連した生殖細胞系列のヘテロ接合型 SEC23B 病的バリアントを有する[Yehia ら 2015, Yehia & Eng 2018] 。生殖細胞系列のヘテロ接合型WWP1異常活性型バリアントが、少数のポリポーシスおよび/または大腸がんを発症したCSおよびCLS患者の一部で同定されている[Lee ら 2020]。活性型WWP1病的バリアントは酵素の異常な活性化をもたらしてPTENを不活性化し、それにより、PTENの機能喪失に類似する、過活動的な成長を促進するPI3Kシグナル伝達を誘発する。その他の遺伝子でわかったことについては、Yehia & Eng [2020]に詳細が記載されている。
臨床的マネジメント
最初の診断後の評価項目
PTEN過誤腫症候群(PHTS)と診断された患者のニーズと疾患の 程度 を確定するためには、 表4にまとめた 評価が推奨される(診断時の評価として実施していない場合)。PHTSの最も深刻な点は、乳房・甲状腺・子宮内膜・腎および程度は少ないが結腸のがんのリスクを高めることにある。それゆえ、PTEN 病的バリアントを有する者のすべてにおいて、マネジメントの最重要点は、腫瘍を早く、最も扱いやすい段階で見つけるために、がんのサーベイランスを強化することにある。年齢に応じた、現在示唆されているスクリーニングとサーベイランスの詳細を表4に示す。
表4.PTEN過誤腫症候群と診断された人に対して推奨される評価とサーベイランス
| 器官/関連事項 | 評価とサーベイランス1 |
|---|---|
| 全般 |
|
| 乳房(女性) |
|
| 甲状腺 | 診断がついた時から (甲状腺がんの最年少報告は7歳): 1年ごとの甲状腺超音波検査 |
| 腎臓 |
|
| 子宮内膜 |
|
| 結腸 | 35歳から 2: 5年ごとの大腸内視鏡; 症状があったり、ポリープが見つかれば間隔を狭める |
| 皮膚 | 1年ごとの皮膚科的評価が推奨される (皮膚悪性黒色腫を含む) |
| 発達 |
|
| 遺伝カウンセリング |
|
MOI=遺伝形式、PHTS=PTEN過誤腫症候群
- NCCNガイドライン®のGenetic/Familial High-Risk Assessment: Breast and Ovarian V.1.2021. © 2021 National Comprehensive Cancer Network, Inc. All rights reserved.から許可を得て転載。ここに掲載されているNCCNガイドラインおよび図版は、NCCNの書面による明示的な許可なしに、いかなる目的でも複製することはできない。2020年12月27日時点。最新のガイドラインの全文を閲覧するには、NCCN.org(無料登録とログインが必要)にアクセスすること。NCCNは、それらの内容、使用、応用に関していかなる保証も行わず、それらの応用や使用に関していかなる責任も負わない。
- 特定のがん種においてより若年発症の家族歴がある場合、家系内で最も若く診断された年齢より5-10歳早くからのスクリーニングを考慮するべきである。
- 臨床遺伝専門医、認定遺伝カウンセラーまたは認定遺伝看護専門看護師
Bannayan-Riley-Ruvalcaba症候群(BRRS)
注:BRRSに対するスクリーニングの推奨事項は確立されていない。しかしながら、最近の分子疫学的研究では、生殖細胞系列PTEN 病的バリアントを有するBRRS患者は、CS患者と同様のサーベイランス(表4参照) を受けるべきとしている。BRRS患者は特に、消化管過誤腫性ポリポーシスおよび低血圧症や側弯症などの筋骨格系の症状に関する合併症を確認するべきである。
Proteus症候群/Proteus様症候群
注:Proteus症候群やProteus様症候群の臨床診断基準を満たす患者の少数に、生殖細胞系列PTEN 病的バリアントが認められたのは比較的最近のことではあるが、これらの疾患患者で生殖細胞系列PTEN 病的バリアントを有する者に対しては、上記のサーベイランス推奨事項を検討すべきである。
症状に対する治療
表5 Cowden症候群およびBannayan-Riley-Ruvalcaba症候群の症状に対する治療
| 症状関連事項 | 治療 | 理由その他 |
|---|---|---|
| 粘膜皮膚病変 | 無症候性病変: 慎重に経過観察 | 皮膚病変は悪性腫瘍が疑われるあるいは症状(痛み、変形、瘢痕化など)が顕著な場合に限り切除する。 |
| 症候性病変: 局所薬(例えば5-フルオロウラシル)、掻爬術、凍結外科手術またはレーザー切断によって、一時的に緩和できる可能性がある[Hildenbrandら 2001]。 | 外科的切除は、ケロイドの形成や病変の再発(しばしば急速に起こる)により複雑化することがある[Eng, 未発表データ] | |
| 発達遅延 | 必要に応じて:
|
|
| 乳房疾患/腫瘍 | 乳がん専門医による治療 | |
| 甲状腺疾患 |
|
甲状腺の亜全摘術では、がんのリスクが残る。 |
| 子宮内膜疾患 | 多発する子宮筋腫は、腹式子宮全摘術で治療する。 | 筋腫のみ切除すると劇的再発が起こりうる。 |
| 消化管腫瘍 | 消化器専門医による内視鏡検査とポリープの除去 | |
| 腎細胞がん | 標準治療 |
Proteus症候群/Proteus様症候群
生殖細胞系列PTEN 病的バリアントを有する者に対しては、CSと BRRSに対するマネジメント推奨事項(表5参照)に従うべきである。Proteus 症候群、マネジメントの項も参照のこと。
主な症状に対する予防
乳がんのリスクの高い女性は、特に乳房組織が高密度であったり、乳房の生検を複数回必要とする場合には、予防的乳房切除を検討する。高リスクの女性では、予防的乳房切除によって乳がんのリスクが90%軽減される[Hartmannら 1999]。注 :予防的乳房切除の推奨は、PHTSのみならず様々な原因により乳がんのリスクが 高い女性に対して一般的に適用される。
PHTS患者の乳がんの発症リスクを低減させる目的でタモキシフェンやラロキシフェンなどの薬剤の日常使用を支持する直接的な証拠は存在しない。医師は証拠の限界と化学 的予防のリスクとベネフィットについて、それぞれの患者と話す必要がある。さらに、既に子宮内膜がんのリスクが高い患者がタモキシフェンを使用した場合に、子宮内膜がんのリスクが上昇することについても話さなければならない。
避けるべき化学物質および環境
急速な組織の再増殖やケロイド組織の形成が起こる傾向があるため、 皮膚病変の切除は悪性が疑われる場合や症状(例、痛み、変形)が顕著な場合にのみ実施することが推奨される。
リスクのある 血縁者の評価
罹患者のリスクの高い血縁者の遺伝的状態を明らかにするために、発端者で同定されたPTEN 病的バリアントの分子遺伝学的検査を行うことが適切である。家系特異的な PTEN病的バリアントを有する(すなわちPHTSの)家系員 は、初期評価と 継続的なサーベイランスを受ける必要がある。
BRRSとProteus症候群は若年で発症する可能性があるため、18歳未満のリスクのある 血縁者に対して分子遺伝学的検査が適している。PHTS患者で報告されている乳がんの最少年齢は17歳、甲状腺がんは7 歳 である。
PTEN 病的バリアントを受け継いでいない 家系員 およびその子孫の がんのリスクは 、一般集団と同様である。
遺伝カウンセリングを目的としたリスクのある 血縁者の検査に関わる問題は、遺伝カウンセリングの項を参照のこと。
現在研究中の治療
mTOR阻害薬 が生殖細胞 PTEN 病的バリアントをもつ患者における悪性腫瘍の治療の見込みを示してはいるものの、その使用は臨床試験に限定すべきである。成人PTHSを対象とした mTOR阻害薬シロリムスの第Ⅱ相オープン臨床試験(NCT00971789)が実施され、試験期間を通して症状を改善させるエビデンスが示された[Komiya ら2019]。 もう1つの、
生殖細胞 PTEN 病的バリアントおよび自閉症スペクトラム障害を有する小児、青少年、および若年成人を対象としたmTOR阻害薬エベロリムスの二重盲検クロスオーバー臨床試験が完了した(NCT02461446) 。
広範な疾患や症状の臨床研究に関する情報は, アメリカでは ClinicalTrials.gov を, ヨーロッパでは EU Clinical Trials Register を参照のこと 。
遺伝カウンセリング
「遺伝カウンセリングは個人や家族に対して遺伝性疾患の本質,遺伝,健康上の影響などの情報を提供し,彼らが医療上あるいは個人的な決断を下すのを援助するプロセスである.以下の項目では遺伝的なリスク評価や家族の遺伝学的状況を明らかにするための家族歴の評価,遺伝学的検査について論じる.この項は個々の当事者が直面しうる個人的あるいは文化的、倫理的な問題に言及しようと意図するものではないし,遺伝専門家へのコンサルトの代用となるものでもない.」
遺伝形式
Cowden症候群およびBannayan-Riley-Ruvalcaba症候群はPTEN 病的バリアントの遺伝またはde novo(新たな)変異 によって生じる、常染色体優性遺伝 性疾患である。
PTEN関連Proteus症候群およびProteus様症候群も常染色体優性遺伝性疾患であるが、ほとんどがde novo(新たな)病的バリアントによって生じる。
患者家族のリスク
発端者の両親
- Cowden症候群(CS). CSは過小診断されやすいため、孤発例(明らかな家族歴がない患者と定義)と家族例( 二人以上の患者がいると定義)の実際の割合は決定できない。 臨床経験に基づくと、 約50%のCS患者 には罹患した血縁者が1人いる[ 著者、未発表データ]。de novo(新たな)病的バリアントはPHTS発端者の10-44%で見つかっている[Mester & Eng 2012] 。
- Bannayan-Riley-Ruvalcab症候群 (BRRS). 大部分のエビデンスは、PTENの病原性バリアントがBRRSの孤発例および家族例の両方に存在することを示唆している [Mester & Eng 2012, Yehia & Eng 2018 ]。
- PTEN関連Proteus症候群とProteus様症候群. 事実上すべての患者がde novo(新たな)病的バリアントを有する 。
- 家族内に罹患者が発端者1人のみの場合、発端者の両親に対して、遺伝的状態を確認し、確実な再発リスクのカウンセリングを実施するために、分子遺伝学的検査が推奨される。
- 発端者で病的バリアントが同定され、両親ともバリアントが見つからなかった場合、以下のことを考慮する必要がある:
- 発端者はde novo(新たな)病的バリアントを有している。注:病的バリアントがde novoと報告されるのは、(1)親のDNAに病的バリアントが同定されず、(2)親が生物学的な母親と父親と確認できている場合である。両親 と患者との間での血縁関係の確認が行われていない場合は、“assumed de novo”(おそらくde novo)と報告される[Richards ら 2015]。
- 性腺(または体細胞+性腺)モザイクの片方の親から、病的バリアントが遺伝した。*注:親の白血球DNAの検査では、体細胞モザイクは検出できない可能性がある。
* PTEN病的バリアントの体細胞+性腺モザイクの親は、軽度/最小限の影響を受ける可能性がある。
- 家系員が疾患を認識していない、あるいは発症前に親が若くして亡くなる、ヘテロ接合性の親がいても発症が遅いなどの理由により、 多くのPTEN過誤腫症候群(PHTS)患者において家族歴がないように見える。それゆえ、分子遺伝学検査を実施して、発端者で同定された病的バリアントを両親で確認しない限り、明らかに家族歴がないとは言い切れない。
発端者の同胞
発端者の同胞のリスクは両親の遺伝学的状況に依存している。
- 発端者の親がPTEN 病的バリアントを有する場合、兄弟姉妹にその バリアントが遺伝するリスクは50%である。PTEN病的バリアントを有する者のPHTSの浸透率は、30歳までで99%である。
- 発端者で検出された PTEN 病的バリアントがいずれの親の白血球DNAにも認められない場合でも、親の性腺モザイクの可能性があるため、 同胞の再発リスクは一般集団よりはやや高くなる[Pritchardら 2013]。
- 両親がPTEN 病的バリアントの検査をしておらず、 30歳代で 臨床的に 罹患していない場合、 兄弟姉妹のリスク は低いように思われる。しかしながら、臨床的に非罹患の両親を持つ発端者の兄弟姉妹は、ヘテロ接合性の親における年齢的浸透率や性腺モザイクの可能性があるため、PHTSのリスクは高まると考えらえる。
発端者の子
- PHTS患者の子はそれぞれ50%の確率でPTEN 病的バリアントを受け継ぐ。
発端者の他の家族
他の 血縁者のリスクは発端者の両親の遺伝学的状況に依存する。一方の親がPTEN 病的バリアントを有する場合、その家系の 血縁者にはリスクがある。
遺伝カウンセリングに関連した問題
早期診断と治療を目的とした、リスクのある 血縁者の検査に関する情報は、 マネジメント、 血縁者に対する評価の項を参照のこと。
無症状の家系員に対する発症前診断では、 家系内に事前に生殖細胞系列PTEN 病的バリアントが同定されている 必要がある。
がん発症リスク評価とカウンセリング. 分子遺伝学的検査を用いる場合や用いない場合の、がん発症リスク評価によるリスクのある個人の同定に関する医学的、心理社会 的、倫理的な様々な問題の包括的な説明は、「がんの遺伝的リスク評価とカウンセリング―医療従事者用」 (Cancer Genetics Risk Assessment and Counseling – for health professionals) (国立がん研究所のPDQ®の一部)を参照のこと。
家族計画.
- 遺伝的リスクを決定し、出生前/着床前診断の利用を検討するための最適な時期は妊娠前である。
- 罹患した、または罹患のリスクがある若年成人に対して遺伝カウンセリング(子供の潜在的リスクと妊娠の選択肢の検討を含む)を提供することは適切である。
DNAバンキング は将来の利用に備えてDNA(通常、白血球から抽出)を保管する。検査法や遺伝子、 バリアント、疾患に関する理解は将来 改善すると思われるため、 患者のDNAの保管について考慮すべきである。
出生前診断と着床前診断
罹患した家系員にPTEN 病的バリアントが同定されたなら、 出生前診断と着床前診断を受けること が可能 である。
医療の専門家の間や家族内においても、出生前診断に対する考え方の相違が存在しうる。ほとんどの施設では出生前診断を行うか否かの決断は両親に委ねているが、この問題に関しては議論することが適切である。
(訳注:日本ではPTEN過誤腫症候群における着床前診断および出生前診断は行われていない)
資源
GeneReviewsスタッフは、この疾患を持つ患者および家族に役立つ以下の疾患特異的な支援団体/上部支援団体/登録を選択した。GeneReviewsは、他の組織によって提供される情報には責任をもたない。選択基準における情報については、ここをクリック。
- MedlinePlus
- My46 Trait Profile
- PTEN Hamartoma Tumor Syndrome Foundation
The PTEN Hamartoma Tumor Syndrome Foundation はPTEN症候群についての教育、患者への財政支援、研究支援、啓蒙活動を目的として設立された。
Email: ptensyndromefoundation@gmail.com
www.ptenfoundation.org
- PTEN Italia
Via San Giuseppe Cottolegno, 36
20143 Milano
Italy
Email: info@ptenitalia.org
www.ptenitalia.org
- PTEN Research
3rd Floor, Paternoster House
London EC4M 8AB
United Kingdom
Email: contact@ptenresearch.org
www.ptenresearch.org
- American Cancer Society (ACS)
250 Williams Street Northwest
Atlanta GA 30303
Phone: 800-227-2345 (toll-free 24/7); 866-228-4327 (toll-free 24/7 TTY)
www.cancer.org
- CancerCare
275 Seventh Avenue
22nd Floor
New York NY 10001
Phone: 800-813-4673 (toll-free); 212-712-8400 (administrative)
Fax: 212-712-8495
Email: info@cancercare.org
www.cancercare.org
- International Society for Gastrointestinal Hereditary Tumours (InSiGHT)
- National Breast Cancer Coalition (NBCC)
乳がん患者やサバイバーのために公共政策の変更を求める支援団体
1101 17th Street Northwest
Suite 1300
Washington DC 20036
Phone: 800-622-2838 (toll-free); 202-296-7477
Fax: 202-265-6854
Email: info@stopbreastcancer.org
www.stopbreastcancer.org
- National Coalition for Cancer Survivorship (NCCS)
すべてのがん患者を支援するための消費者団体
8455 Colesville Road
Suite 930
Silver Spring MD 20910
Phone: 877-622-7937 (toll-free); 301-650-9127
Fax: 301-565-9670
Email: info@canceradvocacy.org
www.canceradvocacy.org
- Susan G. Komen Breast Cancer Foundation
情報、治療センターの紹介。最近診断された女性からの質問に答え、心理的な支援を提供する。医療サービスやサポートが十分でない女性のための研究プログラムに資金を提供。
Phone: 877-465-6636 (Toll-free Helpline)
Fax: 972-855-1605
Email: helpline@komen.org
www.komen.org
分子遺伝学
分子遺伝学とOMIMの表の情報はGeneReviewsの他の場所の情報とは異なるかもしれない。表は、より最新の情報を含むことがある。
Table A. PTEN過誤腫症候群: 遺伝子およびデータベース
| 遺伝子 | 染色体 座位 | タンパク質 | 遺伝子座位特異的データベース | HGMD | ClinVar |
|---|---|---|---|---|---|
| PTEN | 10q23.31 | ホスファチジルイノシトール 3,4,5- 三リン酸3ホスファターゼおよび二重特異性タンパク質ホスファターゼ PTEN | PTE データベース | PTEN | PTEN |
データは以下の標準的参照資料をもとに作成した。遺伝子はHGNC、染色体 座位、遺伝子座位 はOMIM、タンパク質はUniProtを参照した。リンクが提供されたデータベース(遺伝子座位特異的データベース、 HGMD,ClinVar)の記述についてはこちらを参照のこと。
Table B. PTEN 過誤腫症候群 に関するOMIMの情報(全ての情報はOMIMを参照のこと)
| 158350 | COWDEN症候群1; CWS1 |
| 601728 | ホスファターゼとテンシンTENSIN同族体; PTEN |
分子遺伝学的病因
多くの機能研究がなされてきているものの、PTENの完全な機能は未だ十分には理解されていない。PTENは、チロシン、セリンおよびスレオニンからリン酸基を除去する二重特異性ホスファターゼと呼ばれるホスファターゼのサブクラスに属する。また、PTENはホスホイノシチド-3,4,5- 三リン酸の主要なホスファターゼであり、それゆえPI3K/AKT経路を下方制御する[Yehia ら 2019]。
PTENタンパクは、特定の核および細胞質成分に局在する。野生型のタンパク質は、G1細胞周期停止とアポトーシスを引き起こすPI3K/AKT経路を下方制御する、主要な脂質ホスファターゼである。さらに、タンパク質ホスファターゼは、いくつかの細胞サイクリンを下方制御するだけでなく、細胞の移動拡散を阻害する重要な役割もみられる。核のPTENは細胞周期を停止させ、細胞質のPTENはアポトーシスを要求する[Yehia & Eng 2018, Yehia ら 2019]。
PTEN中に見つかっている生殖細胞系列病的バリアントには、ミスセンス/ナンセンス/スプライスサイトバリアント、微細な欠失/挿入、広範囲の欠失がある。現在、150を超える病的バリアントがthe Human Gene Mutation Databaseヒト遺伝子変異データベースに掲載されている(表A参照)。40%近い病的バリアントが、リン酸塩コアモチーフをコードするエクソン5に見つかっている[Yehia ら 2019]。ほとんどの病的バリアントは単独で報告されているが、頻発する病的バリアントも多数報告されている。表6に詳記する。
疾患の発症メカニズム. PTEN生殖細胞系列病的バリアントの大部分(76%)は、PTENタンパク質の切断、欠乏(ハプロ不全)、または機能不全のいずれかに関わると考えられる。多くのミスセンスバリアントは機能せず、いくつかは優性阻害効果を発揮する[Papa ら 2014]。PTENが存在しないか減少するまたは機能しないと、AKT1のリン酸化が阻害されず、細胞周期の停止やアポトーシスの機能不全をもたらす。さらに、ホスファターゼ活性化タンパク質が欠失することで、分裂促進因子活性化タンパク質キナーゼ(MAPK)経路が制御不能となり、異常な細胞生存をもたらす[Yehia ら 2019]。
研究室におけるPTEN特異的な技術的考察. PTENは9番染色体上に、高度に相同性の高い偽遺伝子(PTENP1)が存在する[Dahia ら 1998]。特異性を確保し、この偽遺伝子の相互増幅を避けるために、PTEN特異的なプライマーを設計する際には、特別な配慮が必要となる[Ngeow & Eng 2016]。
表6.有名なPTEN病的バリアント
| 参照配列 | DNA塩基変化 | 予測されるタンパク質の変化 | 解説 [参照] |
|---|---|---|---|
| NM_000314.8 NP_000305.3 |
c.388C>T | p.Arg130Ter | 頻発する病的バリアント [Yehia ら 2019] |
| c.697C>T | p.Arg233Ter | ||
| c.1003C>T | p.Arg335Ter |
表に掲載されているバリアントは著者らによって提供されている。GeneReviewsのスタッフは,バリアントの分類を独自に検証していない.
GeneReviewsは、Human Genome Variation Societyの標準的な命名規則に従っている(varnomen.hgvs.org)。命名法の説明についてはQuick Reference参照。
がんと良性腫瘍
散発性のがんは、しばしば生殖細胞系列ではなくPTENの体細胞バリアントと関連し、PHTSの他の症状のない単独の腫瘍として発症する。体細胞性PTENバリアントおよび遺伝子発現の消失は、子宮内膜がんの類内膜腺がんと前がん病変の類内膜病変(上皮内新生物)によくみられる[Mutter ら 2000]。このような状況では、これらの腫瘍に対する疾病素因(易罹患性)は遺伝性ではない。
更新履歴
-
Gene Review著者:Charis Eng, MD PhD
日本語訳者:中川奈保子,小杉眞司(京都大学大学院医療倫理学)
Gene Review 最終更新日: 2009.5.5. 日本語訳最終更新日:2011.5.22. - Gene Review著者:Charis Eng, MD PhD
日本語訳者:櫻井晃洋(札幌医科大学附属病院遺伝子診療室)
Gene Reviews 最終更新日: 2016.6.2. 日本語訳最終更新日:2017.2.16. - GeneReviews著者: Lamis Yehia, PhD and Charis Eng, MD, PhD.
日本語訳者:箕浦祐子(札幌医科大学大学院医学研究科遺伝医学)櫻井晃洋(札幌医科大学附属病院遺伝子診療科 )
GeneReviews最終更新日: 2021.2.11 日本語訳最終更新日: 2021.3.1[in present]